RESUMEN
Un hombre de 74 años con antecedentes de trasplante renal y terapia reciente con pulsos de corticosteroides ingresó con fiebre y dolor abdominal, inicialmente atribuido a una infección del tracto urinario. Progresó con hemoptisis, disnea e insuficiencia respiratoria, y se le diagnosticó síndrome de hiperinfección por Strongyloides stercoralis, confirmado por biopsia colónica y lavado broncoalveolar, en coinfección con SARS-CoV-2. Se inició tratamiento con ivermectina y albendazol, lo que condujo a la recuperación clínica y la erradicación parasitaria. Cabe destacar que el paciente tenía una parasitología fecal negativa antes del trasplante. La infección por Strongyloides stercoralis es prevalente en regiones tropicales y subtropicales. El diagnóstico es difícil debido a la baja sensibilidad de las pruebas de heces y la disponibilidad limitada de métodos moleculares, que pueden retrasar el tratamiento.
Hyperinfection by Strongyloides stercoralis in a Renal Transplant Patient with SARS-CoV-2 Viral Coinfection
ABSTRACT
A 74-year-old male with a history of kidney transplantation and recent corticosteroid pulse therapy was admitted with fever and abdominal pain, initially attributed to a urinary tract infection. He progressed with hemoptysis, dyspnea, and respiratory failure, and was diagnosed with Strongyloides stercoralis hyperinfection syndrome, confirmed by colonic biopsy and bronchoalveolar lavage, in co-infection with SARS-CoV-2. Treatment with ivermectin and albendazole was initiated, leading to clinical recovery and parasitic eradication. Notably, the patient had a negative stool parasitology prior to transplantation.
Strongyloides stercoralis infection is prevalent in tropical and subtropical regions. Diagnosis is challenging due to the low sensitivity of stool tests and limited availability of molecular methods, which may delay treatment.
INTRODUCCIÓN
La infección por Strongyloides stercoralis constituye un reto diagnóstico en pacientes inmunocomprometidos, especialmente trasplantados de órganos sólidos. La inmunosupresión puede desencadenar formas graves como el síndrome de hiperinfección, con alta mortalidad. El uso de glucocorticoides, incluso en cursos breves, es uno de los principales factores precipitantes. La coinfección con virus respiratorios como SARS-CoV-2 puede, además, agravar el cuadro e interferir en su diagnóstico oportuno, no siendo frecuentemente informada. La sensibilidad limitada de los métodos diagnósticos tradicionales, como el examen parasitológico de materia fecal, dificulta su detección en etapas tempranas. En este contexto se presenta el caso de un paciente con trasplante renal, inmunosupresión crónica y reciente corticoterapia, que desarrolló síndrome de hiperinfección por S. stercoralis asociado a infección viral pulmonar concomitante. El caso destaca la importancia de la vigilancia en regiones endémicas y de estrategias más eficaces para el diagnóstico y prevención en pacientes de riesgo.
CASO CLÍNICO
Paciente masculino de 74 años, oriundo de Paraguay donde residió hasta los 18 años, presenta como antecedente personal enfermedad renal crónica de etiología no filiada, por la cual fue sometido a trasplante renal en junio de 2024. Durante el estudio pretrasplante se documentaron registros aislados de 7900 leucocitos totales y recuento de 32% de eosinófilos; se realizaron dos exámenes parasitológicos seriados, ambos negativos para formas parasitarias. Se interpretó hipereosinofilia de probable origen alérgico.
En marzo de 2025, el paciente presentó episodio de rechazo agudo limítrofe en contexto de caída progresiva del filtrado glomerular, por lo cual requirió internación durante tres días para pulso de metilprednisolona (250 mg/día). Egresó sin complicaciones.
El 19 de marzo reingresó con un cuadro clínico de una semana de evolución, caracterizado por hiporexia, astenia y dolor abdominal difuso, asociado a episodio febril de hasta 39 °C en domicilio. Al ingreso se encontraba en tratamiento con meprednisona 4 mg/día, tacrolimus 2,5 mg/día y everolimus 2 mg cada 12 horas. Los estudios iniciales evidenciaron insuficiencia renal crónica reagudizada y sedimento urinario patológico; el urocultivo desarrolló Escherichia coli y BLEE, y las tomografías de tórax y abdomen mostraron hallazgos compatibles con colitis, interpretándose el cuadro como una infección urinaria complicada, por lo que se inició tratamiento antibiótico empírico con meropenem.
Durante el primer día de internación presentó un episodio de rectorragia, sin compromiso hemodinámico.
Se le realizó videocolonoscopia que evidenció mucosa eritematosa y congestiva, sin sangrado activo. Al noveno día de internación, el paciente desarrolló disnea, taquipnea, deterioro de la mecánica ventilatoria, tos seca y hemoptisis, con desaturación en aire ambiente. La PCR multiplex para virus respiratorios resultó positiva para SARS-CoV-2, rinovirus y enterovirus. La tomografía de tórax mostró infiltrado bilateral difuso de patrón reticulonodulillar (Fig. 1), y el lavado broncoalveolar (BAL) evidenció débito hemático, interpretándose el cuadro como hemorragia alveolar difusa de probable origen infeccioso. Se instauró tratamiento con antibióticos de amplio espectro, remdesivir, corticosteroides en dosis altas, nebulizaciones con ácido tranexámico y soporte ventilatorio con cánula de alto flujo. A pesar de estas medidas, evoluciona desfavorablemente, requiriendo intubación orotraqueal y ventilación mecánica al día 11 de internación.
Al mismo tiempo se obtuvo el informe anatomopatológico de las biopsias colónicas, que revelaron la presencia de nematodos compatibles con Strongyloides stercoralis (Fig. 2). A partir de este hallazgo se revisó la microscopia directa del BAL (Fig. 3), donde también se identificaron formas larvarias. Con base en estos hallazgos, en el día número 13 de internación, se reorienta el diagnóstico hacia un síndrome de hiperinfección por Strongyloides asociado a infección viral concomitante en el contexto de inmunosupresión intensa.
Se inició tratamiento antiparasitario con ivermectina 12 mg/día y albendazol 400 mg cada 12 horas, observándose una evolución clínica favorable con mejoría respiratoria progresiva y extubación sin complicaciones. Completa catorce días de tratamiento rotando a monoterapia con ivermectina 12 mg/día. Luego de esto presenta tres parasitológicos seriados separados por una semana sin formas larvarias evidenciables, por lo que se pasa a ivermectina semanal. El paciente presentó mejoría clínica sostenida y fue dado de alta. En el seguimiento ambulatorio posterior, asistió a un único control por Infectología, en el cual refirió haber continuado con la medicación indicada. Se solicitó un nuevo examen coproparasitológico para evaluar la erradicación parasitaria; sin embargo, el paciente no concurrió a controles posteriores y se perdió el seguimiento clínico a mediano plazo.
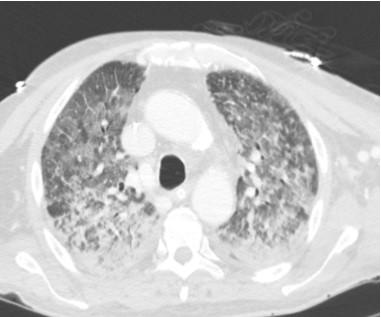
Figura 1. Tomografía de tórax corte axial. Texto alternativo para asistencia visual: tomografía de tórax corte axial por encima de bifurcación de la carina y por debajo del cayado aórtico; se puede observar en ventana de parénquima pulmonar un patrón reticulonodulillar bilateral con predominio de zona posterior y central.
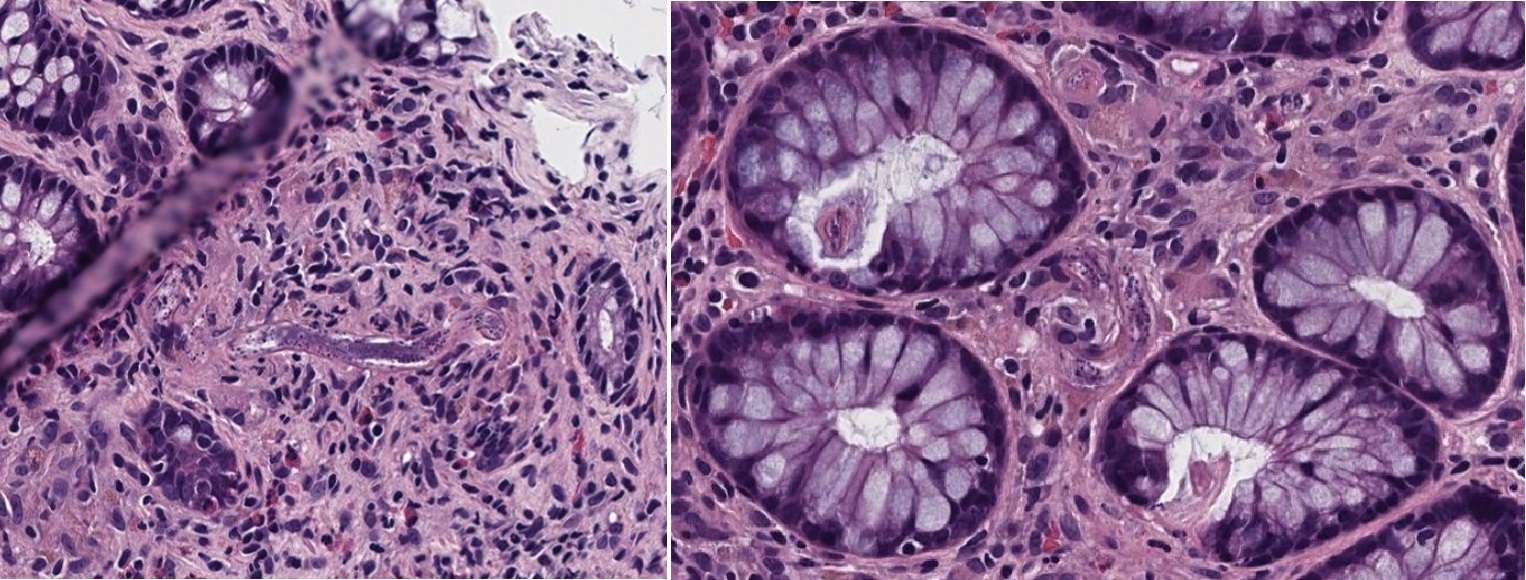
Figura 2. Anatomía patológica de biopsia de colon izquierdo.
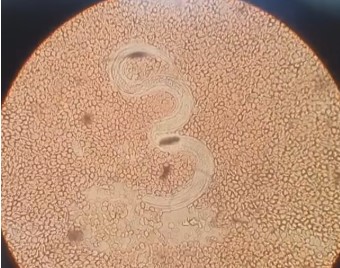
Figura 3. Microscopia directa muestra de lavado broncoalveolar.Texto alternativo para asistencia visual: microscopia directa de muestra obtenida por lavado broncoalveolar; puede observarse estructura de extensión tortuosa bien definida compatible con larva adulta de un nematodo.
DISCUSIÓN
La infección por S. stercoralis afecta a entre 30 y 70 millones de personas en el mundo, y es endémica en aproximadamente 70 países, con predominancia en regiones tropicales y subtropicales1. En América del Sur, su mayor prevalencia se registra en áreas hiperendémicas del sur de Brasil. La transmisión ocurre principalmente por contacto directo de la piel con suelo contaminado, aunque también puede presentarse por vía fecal-oral o interpersonal. A diferencia de otros helmintos, S. stercoralis posee la capacidad de completar un ciclo de autoinfección dentro del hospedador.
En individuos inmunocompetentes, la infección suele ser asintomática, lo que dificulta su diagnóstico.
Sin embargo, en pacientes inmunosuprimidos, pueden desarrollarse formas complicadas, como el síndrome de hiperinfección, caracterizado por una proliferación acelerada de larvas y una mayor migración pulmonarintestinal2. Los factores de riesgo más importantes incluyen el trasplante de órganos sólidos, la infección por HTLV-1 y, principalmente, el uso de glucocorticoides3.
En el caso presentado, el paciente tenía antecedentes de trasplante renal, inmunosupresión crónica y un ciclo reciente de corticoides en alta dosis. Este último factor, además de inducir apoptosis de células Th2 y reducir el recuento de eosinófilos, genera metabolitos hepáticos con actividad similar a la ecdisona –molécula implicada en la oviposición y ecdisis larvaria de los helmintos– lo que puede acelerar el ciclo parasitario y facilitar una diseminación fuera del control inmunológico del hospedador4.
El diagnóstico de esta parasitosis continúa siendo un desafío. Las pruebas directas en materia fecal presentan baja sensibilidad debido a la excreción intermitente y en bajo volumen de larvas. Su rendimiento diagnóstico mejora con la recolección seriada en al menos tres días, y alcanza una sensibilidad de hasta el 90%, en comparación con el 30-40% de una única muestra. En el período pretrasplante, si bien se documentaron coproparasitológicos seriados negativos, no se realizaron pruebas serológicas ni moleculares para Strongyloides stercoralis, fundamentalmente por su limitada disponibilidad en el centro, razón por la cual no figuran dentro del protocolo estándar de búsqueda. En este caso, el diagnóstico fue omitido durante la evaluación pretrasplante, lo que pone de manifiesto una limitación relevante del abordaje diagnóstico en pacientes de alto riesgo. Las técnicas serológicas, si bien ofrecen mayor sensibilidad, pueden presentar reactividad cruzada con otros helmintos y no distinguen infecciones actuales de las pasadas. Por otro lado, las pruebas moleculares se consideran el procedimiento de referencia (estándar de oro), aunque su disponibilidad es limitada en muchos centros.
En relación con el tratamiento, en casos no complicados, la ivermectina en dosis de 200 µcg/kg/día durante dos días ha demostrado ser segura y eficaz, y se recomienda un segundo ciclo a los catorce días en pacientes inmunosuprimidos5. No obstante, en formas complicadas, no existe un consenso claro sobre el régimen óptimo. La evidencia actual sugiere que una combinación de ivermectina (12 mg/día) y mebendazol (400 mg cada 12 horas) durante catorce días puede ser eficaz6, aunque no hay pautas definidas sobre la duración total del tratamiento ni sobre la necesidad de una terapia de mantenimiento. La reducción o suspensión de la inmunosupresión, cuando es posible, es también un componente fundamental del tratamiento.
Respecto de la infección por SARS-CoV-2, se han informado numerosos casos en los que la infección viral desencadena la necesidad de corticoterapia, lo que posteriormente precipita una hiperinfección por S. stercoralis7 . En el presente caso, la detección simultánea de SARS-CoV-2 y del síndrome de hiperinfección plantea la posibilidad de un papel multifactorial del virus, ya sea como desencadenante indirecto a través del refuerzo de la inmunosupresión, como factor agravante del compromiso respiratorio, o como infección coexistente sin un impacto causal directo. Lo destacable es que la instauración del tratamiento antiparasitario coincidió temporalmente con una mejoría clínica sostenida, particularmente respiratoria, lo que sugiere que la carga parasitaria tuvo un papel central en la fisiopatología del cuadro. No obstante, la superposición temporal de ambas infecciones limita la capacidad de atribuir con precisión el peso específico del SARS-CoV-2 en el desenlace clínico, constituyendo una limitación en la interpretación del caso.
CONCLUSIÓN
Este caso resalta la importancia de considerar la infección por Strongyloides stercoralis en pacientes inmunosuprimidos, especialmente ante corticoterapia reciente. La detección temprana y el inicio oportuno del tratamiento antiparasitario pueden modificar favorablemente el pronóstico, incluso en contextos de coinfección con SARSCoV-2. La disponibilidad limitada de métodos diagnósticos continúa siendo un desafío en la práctica clínica.