RESUMEN
Introducción
Los meningoceles y meningoencefaloceles se producen por la hernia de las meninges con o sin tejido encefálico a través de defectos en la base de cráneo. El objetivo fue determinar la tasa de éxito de la reparación de la base del cráneo por meningoceles y menigoencefaloceles mediante un abordaje endonasal asistido con endoscopios, y establecer un algoritmo para el topodiagnóstico preoperatorio de estas lesiones.
Métodos
Se incluyeron los pacientes que fueron tratados por meningoceles y menigoencefaloceles de base de cráneo mediante un abordaje endonasal con endoscopios, entre enero de 2010 y marzo de 2024. La reconstrucción del defecto se realizó con técnica multicapa con injertos autólogos y colgajos locales.
Resultados
Fueron tratados 10 pacientes, 9 con meningoceles y uno con un meningoencefalocele. Tres se localizaron en el seno esfenoidal, seis en la lámina cribosa del etmoides y uno en el seno frontal. La tasa de éxito que obtuvimos en la reparación del defecto en la base del cráneo fue 90%.
Conclusiones
La tasa de éxito que tuvimos en la reparación de la base del cráneo por defectos ocasionados por meningoceles y meningoencefaloceles utilizando un abordaje endonasal fue 90%.
La tomografía computarizada de macizo facial y la resonancia magnética con contraste con protocolo para visualizar el bulbo olfatorio resultó muy útil para diagnosticar el sitio de las lesiones a la altura de la lámina cribosa del etmoides.
Palabras clave: Meningoceles, meningoencefaloceles, cirugía endoscópica, reconstrucción de base de cráneo.
Endonasal Management of Skull Base Defects: Meningoceles and Meningoencephaloceles
ABSTRACT
Introduction
Meningoceles and menigoencephaloceles result from herniation of the meninges, with or without brain tissue, through defects in the skull base.
Objectives
To determine the success rate of skull base repair for meningoceles and menigoencephaloceles using an endonasal approach assisted by endoscopes, and to establish an algorithm for the preoperative topographic diagnosis of these lesions.
Methods
Patients treated for skull base meningoceles and menigoencephaloceles using anendonasal approach assisted by endoscopes between January 2010 and March 2024 wereincluded. Reconstruction of the defect was performed using a multilayer technique withautologous grafts and local flaps.
Results
Ten patients were treated: nine with meningoceles and one with a meningoencephalocele. Three were located in the sphenoid sinus, six in the cribriform plate of the ethmoid bone, and one in the frontal sinus.
The success rate we achieved in repairing the skull base defect was 90%.
Conclusions
The success rate we achieved in repairing skull base defects caused by meningoceles and meningoencephaloceles using an endonasal approach was 90%.
Computed tomography and contrast-enhanced magnetic resonance imaging (MRI) with a protocol to visualize the olfactory bulb were very useful in diagnosing the site of the lesions at the level of the cribriform plate of the ethmoid bone.
Key words: Meningoceles, meningoencephaloceles, endoscopic surgery, skull base reconstruction.
INTRODUCCIÓN
Los meningoceles (MC) y meningoencefaloceles (MEC) son protrusiones de las meninges y de las meninges y de tejido cerebral a través de un defecto óseo en la base del cráneo, hacia la cavidad nasal o senos paranasales, formando una lesión quística con contenido de líquido cefalorraquídeo (LCR).
El tejido cerebral es habitualmente no funcionante.
El defecto en la base del cráneo puede ser congénito o adquirido (presión intracraneal elevada, trauma, tumores expansivos o iatrogénicos por cirugías).
El tratamiento de estas lesiones tiene el objetivo de reparar el defecto óseo para evitar el riesgo de meningitis.
Hay diferentes abordajes quirúrgicos para tratar los MC y MEC.
El acceso endonasal con endoscopios, utilizando la técnica de reconstrucción multicapa con injertos o colgajos es de elección, por su alta tasa eficacia en la reparación y su baja morbilidad.
OBJETIVOS
Determinar la tasa de éxito de la reparación de la base del cráneo por meningoceles y menigoencefaloceles idiopáticos, mediante un abordaje endonasal asistido con endoscopios, y establecer un algoritmo para el topodiagnóstico preoperatorio de estas lesiones.
DISEÑO
Descriptivo y retrospectivo.
MATERIAL Y MÉTODO
Se incluyó la totalidad de los pacientes que fueron tratados por MC y MEC de base de cráneo mediante un abordaje endonasal con endoscopios, entre enero de 2010 y marzo de 2024.
El diagnóstico de craneolicuorrea se confirmó en el intraoperatorio en la mitad de los pacientes y, en la otra mitad, por la determinación preoperatoria de la proteína β-trace.
En todos se realizó una endoscopia nasal, tomografía de macizo facial (TC) y una resonancia de macizo facial con contraste (RM). En casos donde la tomografía no evidenció claramente un defecto óseo en la base del cráneo, la RM fue realizada con el protocolo para visualizar el bulbo olfatorio (secuencias T2 Fast Spin Echo con supresión grasa y la secuencia T2 3D isotrópica de alta resolución que permitió su reformateo multiplanar, optimizando el contraste entre el líquido cefalorraquídeo y la vía olfatoria).
Las cirugías consistieron en exponer las lesiones mediante un acceso endonasal con endoscopios y reducirlas con pinza bipolar. Después se resecó la mucosa circundante al defecto óseo y se hizo la reconstrucción con técnica multicapa con injertos de mucoperiostio septal o cornete y grasa obtenida del lóbulo de la oreja o colgajos locales de cornete medio, inferior o nasoseptal.
Colocamos un adhesivo biológico (cola de fibrina) o un sellador de la duramadre compuesto por un hidrogel sintético con polietilenglicol y polietilenamina (Adherus®), como última capa de reparación y después esponja de gelatina absorbible (Spongostan®) o matriz hemostática (Surgifló™) y un dedo de guante con esponja de acetato de polivinilo hidroxilado (Merocel®) en su interior, como taponaje nasal de sostén durante tres días.
Los pacientes estuvieron internados 3 días hasta la extracción del taponaje nasal.
Los endoscopios utilizados fueron de 0° y el instrumental fue el convencional para cirugía endoscópica rinosinusal. No se utilizó neuronavegador.
El protocolo del presente estudio fue aprobado por el Comité de Ética institucional del Hospital Italiano de Buenos Aires (aprobación 7485, número de expediente Priisa:16207) y fue conducido de acuerdo con los lineamientos asentados por la declaración modificada de Helsinki.
RESULTADOS
Fueron tratados 10 pacientes, 9 con MC y uno con un MEC.
Ocho fueron mujeres y dos fueron hombres.
Ocho tuvieron fístulas con débito intermitente.
La etiología de los defectos fue idiopática (ningún paciente tuvo antecedentes de traumas, cirugías previas u otras lesiones en cavidad nasal y senos paranasales).
Tres se localizaron en el seno esfenoidal, 2 en la pared lateral y uno en el plano esfenoidal.
En uno usamos fluoresceína intratecal (se extrajeron 10 mL de LCR por punción lumbar y se mezclaron con 0,2 mL de fluoresceína al 5%; se inyectó 1 mL por minuto).
El abordaje se realizó mediante esfenoidotomía bilateral en dos pacientes y en uno mediante un acceso transpterigoideo y esfenoidotomía.
La reconstrucción fue multicapa con injertos. Se colocó un drenaje lumbar en una paciente, porque tuvo la presión intracraneal elevada.
En un enfermo la reparación fracasó a los 4 meses y fue tratada con éxito mediante una craneotomía temporal y reconstrucción del defecto (Fig. 1).
Seis tuvieron MC localizados en la lámina cribosa del etmoides.
En 5 de 6 pacientes se confirmó el topodiagnóstico de MC y craneoliquorrea mediante RM con protocolo para ver el bulbo olfatorio. En todos se resolvió la licuorrea (Fig. 2).
Un paciente tuvo un MEC en el seno frontal izquierdo y fue tratado con éxito mediante un abordaje endonasal al seno frontal tipo Draf III. El defecto se reparó con técnica multicapa (Fig. 3).
La tasa de éxito que obtuvimos en la reparación del defecto en la base del cráneo fue 90% (Tabla 1).
DISCUSIÓN
La etiología de los MC y MEC puede ser traumática, iatrogénica, congénita o idiopática. Esta última está relacionada con un posible aumento de la presión intracraneal (> de 25 cm H2O). La patofisiología no es bien conocida, pero se produciría por una hipertensión venosa que alteraría la reabsorción del LCR por las vellosidades aracnoideas.
También la sobreproducción de LCR podría contribuir a la elevación de la presión intracraneal1 .
Los defectos se producirían por afinamiento del hueso de la base del cráneo en zonas adyacentes a la duramadre pulsátil, senos venosos o granulaciones aracnoideas que repetidamente impactan contra el hueso y producen dehiscencias, meningoceles y fístulas de LCR.
Estas lesiones son más comunes en mujeres obesas (alteración del retorno venoso cerebral por aumento de la adiposidad abdominal)2 y en pacientes con apneas del sueño (la hipoventilación produce hipercarbia que ocasiona vasodilatación cerebral e hipertensión venosa)3.
En nuestro estudio predominaron las mujeres (8/10) y 6 fueron obesas (> 30 de índice de masa corporal).
La estenosis de los senos venosos durales también ha sido asociada con elaumento de la presión intracraneal4.
Los defectos y la hernia de tejido dural y encefálico se produce con más frecuencia en zonas de debilidad ósea como: el techo etmoidal, lámina cribosa, hendidura olfatoria, receso lateral del esfenoides (lateral al canal del nervio vidiano y agujero redondo)5- 7.
En nuestra serie fueron más frecuentes las lesiones localizadas a la altura de la lámina cribosa/hendidura olfatoria (6/10).
En algunos pacientes pueden existir múltiples defectos en la base del cráneo8.
El diagnóstico de una fístula de líquido cefalorraquídeo tiene dos objetivos: determinar si la rinorrea acuosa es líquido cefalorraquídeo y el topodiagnóstico del defecto óseo en la base de cráneo que origina la pérdida de líquido.
El primer objetivo lo podemos determinar mediante la medición de la proteína b-trace en el LCR. Esta proteína se encuentra en el LCR, y puede medirse en suero y orina. La otra posibilidad es la medición en el líquido que sale por nariz de β2 transferrina9.
Mediante estas mediciones se puede detectar 5 uL y 100 uL de líquido cefalorraquídeo en 1 mL de secreción nasal mediante dosaje de β-trace y β2 transferrina, respectivamente10.
El dosaje β2 transferrina tiene una sensibilidad y especificidad superiores al 90%, mientras que la proteína β-trace es más rápida y económica de procesar y se presenta en una concentración más alta que en el suero, lo que la convierte en un marcador excelente de LCR (sensibilidad superior al 90% y especificidad del 100%)11.
En cuatro de los pacientes descriptos se confirmó previamente la presencia de líquido cefalorraquídeo en la rinorrea mediante el dosaje de la proteína b-trace.
Este estudio no se realizaba en nuestro país antes del año 201512.
La localización del sitio de la fístula se realiza mediante endoscopia nasal en consultorio (solo identificamos el sitio de la fístula en un solo paciente con un meningoencefalocele frontal) y con imágenes.
La tomografía computarizada de macizo facial sin contraste con cortes finos puede identificar defectos óseos a nivel del techo etmoidal, esfenoides o frontal, un nivel líquido en el seno esfenoidal por acumulación de LCR o una protrusión de las meninges en la cavidad nasal.
Cuando por tomografía no se identificó el sitio de la fístula (más frecuente sucedió a la altura de la lámina cribosa) fue importante la evaluación con resonanciamagnética con contraste, utilizando el protocolo para evaluar el bulbo olfatorio.
La comparación de la señal en FLAIR y CISS puede ayudar a diferenciar entre el LCR (brillante en CISS, oscuro en FLAIR) y la inflamación/edema (brillante en CISS, brillante en FLAIR)13,14 (Fig. 4A, 4B, 4C).
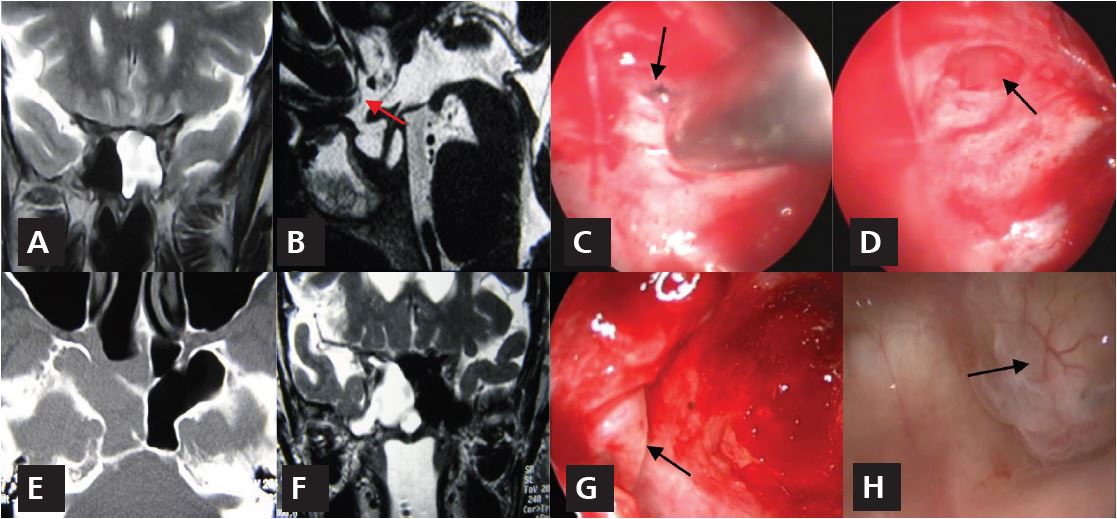
Figura 1. Meningoceles localizados en el plano esfenoidal y seno esfenoidal con fístula de LCR de alto débito. Meningocele plano esfenoidal. A: RM donde se observa acumulación de LCR en esfenoides izquierdo, B: RM de perfil donde se ve la salida del LCR con contraste a través del defecto en el plano esfenoidal (flecha). C: visión endonasal con endoscopio después de la esfenoidotomía y reducción con bipolar del meningocele (flecha). D: defecto después de resecar la mucosa circundante (flecha). Meningocele en pared lateral derecha del esfenoides. E: TC que muestra el seno esfenoidal derecho neumatizado lateralmente y ocupado, F: ocupación del seno esfenoidal derecho por LCR, G: meningocele esfenoidal lateral (flecha). H: meningocele esfenoidal localizado en pared lateral izquierda del seno esfenoidal (flecha).
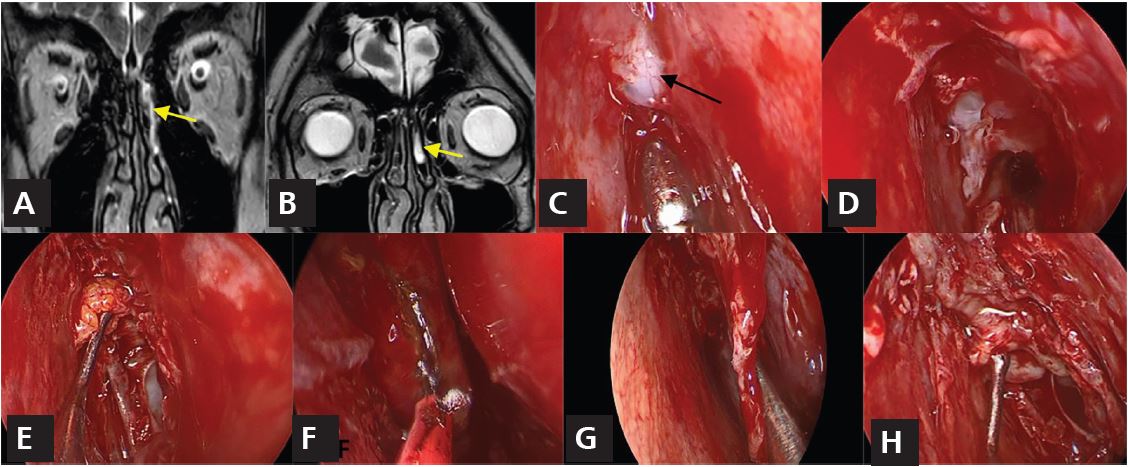
Figura 2. Meningocele localizado a la altura del techo etmoidal. A y B: RM con protocolo para visualizar el bulbo olfatorio; se observa la salida de LCR (flecha) y acumulación dentro del cornete (flecha). C: visión endonasal con endoscopios de meningocele etmoidal (flecha). D: visión después de reducir el meningocele con bipolar. E: colocación de grasa autóloga intracraneal/extradural. F: disección del colgajo de cornete medio con bisturí monopolar y resección de la mitad medial. G: rotación de la mitad lateral del cornete hacia el defecto. H: reparación del defecto en la base de cráneo con el colgajo rotatorio de cornete medio.
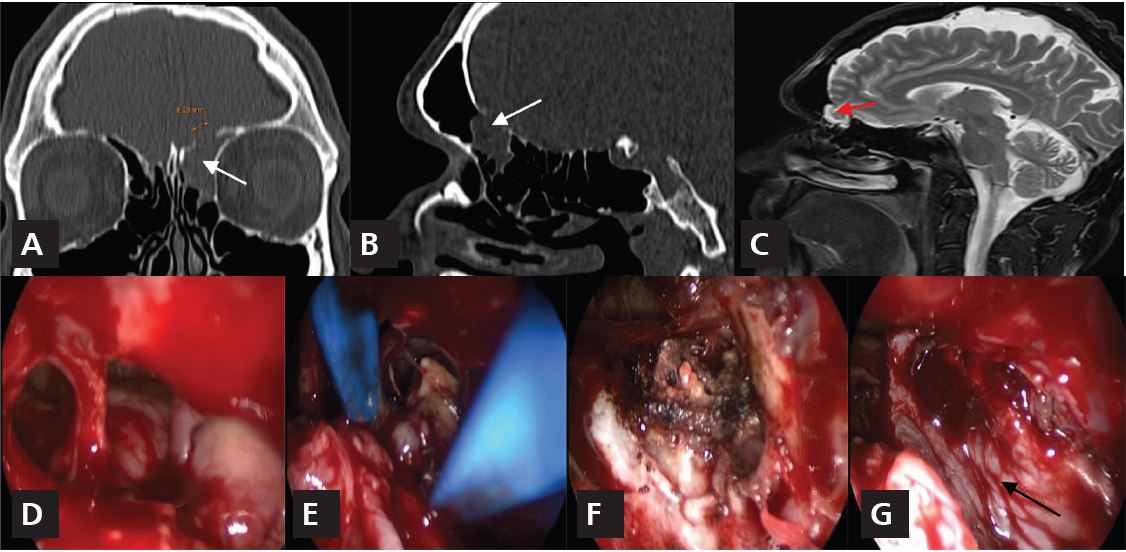
Figura 3. Meningoencefalocele del seno frontal izquierdo. A y B: tomografía computarizada corte coronal y perfil, donde se observa un defecto óseo con protrusión de tejido cerebral (flechas). C: RM donde se ve el meningoencefalocele en el seno frontal (flecha). D: exposición del meningoencefalocele mediante un abordaje endonasal con endoscopio extendido al seno frontal (Draf-III). E: reducción del meningoencefalocele con pinza bipolar. F: visión del defecto para reparar, G: reconstrucción multicapa con colgajo nasoseptal (flecha).
Tabla 1. Pacientes tratados mediante un abordaje endonasal con asistencia de endoscopios por meningoceles y meningoencefaloceles de base de cráneo.
| Edad | Sexo | Localización | Tipo de lesión y tamaño lumbar | Cirugía: reconstrucción | Drenaje | Éxito | Tiempo de seguimiento |
|---|---|---|---|---|---|---|---|
| 64 | F | Esfenoide lateral | Meningocele (10 mm) | Técnica multicapa (fracaso de 2 cirugías endonasales), luego cierre por craneotomía | No | No | 4 meses (hasta que se realizó la reparación por craneotomía) |
| 59 | F | Esfenoides pared lateral | Meningocele (15 mm) | Injerto de mucoperiostio over y grasa esfenoidal | No | Sí | Sin craneolicuorrea por 84 meses |
| 54 | F | Plano esfenoidal | Meningocele (0,8 mm) | Cartílago intracraneal/extradural + injerto mucoperiostio septal | Sí | Sí | 10 meses |
| 48 | H | Seno frontal | Meningoencefalocele (19 mm) | Cartílago intracraneal/extradural + colgajo nasoseptal | No | Sí | 8 meses |
| 62 | F | Lámina cribosa de etmoides izquierda | Meningocele (0,8 mm) | Grasa intracraneal/extradural + colgajo de cornete medio | No | Sí | 7 meses |
| 27 | H | Lámina cribosa de etmoides derecha | Meningocele (0,7 mm) | Grasa intracraneal/extradural + colgajo de pared lateral nasal | No | Sí | 80 meses |
| 34 | F | Lámina cribosa de etmoides izquierda | Meningocele (0,8 mm) | Grasa intracraneal/extradural + colgajo de cornete medio | No | Sí | 10 meses |
| 37 | F | Lámina cribosa de etmoides derecha | Meningocele (0,7 mm) | Grasa intracraneal/extradural + colgajo de cornete medio | No | Sí | 15 meses |
| 52 | F | Lámina cribosa de etmoides izquierda | Meningocele (0,8 mm) | Grasa intracraneal/extradural + injerto de mucoperiostio de cornete medio | No | Sí | 46 meses |
| 65 | F | Lámina cribosa de etmoides izquierda | Meningocele (0,8 mm) | Grasa intracraneal/extradural + colgajo de cornete medio | No | Sí | 12 meses |
ALGORITMO DIAGNÓSTICO DE LICUORREA NASAL Y TOPODIAGNÓSTICO DEL DEFECTO EN BASE DE CRÁNEO
Las imágenes también pueden identificar signos indirectos de hipertensión endocraneal: silla turca vacía, ventrículos laterales dilatados, aumento de la tortuosidad del nervio óptico, distensión del espacio subaracnoideo perióptico (se visualiza un amplio anillo de LCR alrededor del nervio óptico)15. En las imágenes de ninguno de los pacientes descriptos hallamos signos indirectos de presión intracraneal elevada.
En nueve pacientes pudimos localizar previamente a la cirugía el sitio probable del meningocele/meningoencefalocele. En un solo enfermo con antecedentes de cirugías abiertas donde no pudieron localizar el defecto, utilizamos la inyección previa de fluoresceína intratecal.
No nos fue útil porque al realizar la esfenoidotomía pudimos detectar el meningocele en la pared lateral del seno esfenoidal sin inconvenientes.
El abordaje endonasal con endoscopios es la técnica quirúrgica de elección para tratar MC y MEC con proyección rinosinusal.
Hay consenso en reparar el defecto óseo en la base del cráneo lo antes posible16,17.
La reducción con pinza bipolar del MC/MEC y la resección de la mucosa que circunda al defecto óseo son pasos comunes en todas las cirugías.
La reconstrucción multicapa es siempre preferible en los sectores en donde esto puede ser posible (en la lámina cribosa es difícil colocar un injerto intracraneal intradural sin lesionar las fibras del nervio olfatorio y aumentar el tamaño del defecto).
La reconstrucción de defectos menores de 2 cm y de bajo flujo puede ser realizada con injertos autólogos obtenidos preferentemente del mucoperiostio septal contralateral o del cornete medio, con un resultado similar que con colgajos locales.
Cuando el defecto está en el etmoides preferimos usar el colgajo bipediculado de cornete medio y para otras localizaciones el colgajo nasoseptal o el de pared lateral con pedículo anterior o posterior. Como primera capa de reconstrucción (intracraneal-extradural) preferimos usar grasa obtenida del abdomen o del lóbulo de la oreja).
La utilización de un drenaje lumbar en fístulas idiopáticas es controvertida. En un consenso internacional sobre las conductas para seguir en fístulas idiopáticas de líquido cefalorraquídeo, se llegó a un acuerdo del 59% en que el uso de un drenaje lumbar puede ser necesario para inyectar fluoresceína preoperatoria, para medir la presión intracraneal y para reducirla después de la reparación de la base del cráneo10. En otra revisión informaron que trataron de evitar el drenaje lumbar siempre que fue posible, salvo en fístulas de alto flujo, y cirugías de revisión18.
En un estudio prospectivo evaluaron 150 pacientes: al 50% se le colocó un drenaje lumbar en el mismo tiempo de la cirugía para reparar la fístula de LCR. La tasa de éxito de la reparación fue 77% para fístulas espontáneas versus 96-97% para las iatrogénicas y traumáticas.
Concluyeron que el drenaje lumbar no disminuía la tasa de recurrencia en pacientes con presión intracraneal elevada19. En otros estudios también consideraron que el drenaje lumbar no es de uso rutinario en todas las fístulas de LCR20, 21.
En nuestra serie usamos un drenaje lumbar posoperatorio en una paciente con un MC localizado en el techo del esfenoides que tenía la presión intracraneal elevada y un débito de alto flujo. Creemos que el drenaje lumbar puede ser útil en fístulas de alto flujo, cirugías de revisión y cuando se diagnostican en las imágenes signos de presión intracraneal elevada.
En una revisión publicada en Medline que incluyó 1178 pacientes, compararon los resultados de la reparación de la base de cráneo por MC y MEC, utilizando un abordaje endonasal con endoscopios y mediante una cirugía por vía externa.
No hallaron diferencias significativas en el éxito de la reparación (90%) entre los dos abordajes.
Las complicaciones fueron significativamente más bajas en los pacientes tratados por vía endonasal (meningitis 3,9% versus 1,1%, absceso o infección de la herida 6,8% versus 0,7%, y sepsis 3,9% versus 0%). La mortalidad perioperatoria fue también más baja en el grupo tratado por un acceso endonasal: 0% versus 1,4% para el abordaje externo.
Concluyeron que el abordaje endonasal con endoscopios es una técnica segura y eficaz22.
En un estudio describieron 17 pacientes con meningoencefaloceles de fosa craneal anterior y región paraselar que fueron tratados mediante cirugía endoscópica. En 15, la reparación fue exitosa con la primera cirugía y en dos con una fístula persistente asociada a hidrocéfalo con una segunda intervención y la colocación de una derivación ventriculoperitoneal23.
En otro estudio sobre 141 pacientes tratados por meningoceles o menigoencefaloceles por vía endonasal con endoscopios, informaron un 96,5% de éxito en la reparación de la base del cráneo24. La tasa de éxito en la reparación de los defectos en la base del cráneo que obtuvimos en los pacientes descriptos (90%) fue similar a la de los estudios mencionados previamente.
Otras posibilidades que pueden sumarse a la reparación quirúrgica para evitar recurrencias son: la reducción de peso en pacientes obesos, el tratamiento de la apnea obstructiva del sueño y la colocación de endoprótesis (stents) en los senos venosos durales, con más frecuencia sigmoideo y transverso25.

Figura 4. A. Algoritmo diagnóstico en defectos de la base del cráneo. B, C. RM con protocolo para estudio del bulbo olfatorio, donde se observa la salida de LCR y acumulación en celdas etmoidales anteriores izquierdas (entre flechas verdes).
CONCLUSIONES
La tasa de éxito que tuvimos en la reparación de la base del cráneo a causa de defectos ocasionados por meningoceles y meningoencefaloceles utilizando un abordaje endonasal fue 90%.
La tomografía computarizada de macizo facial y la resonancia magnética con contraste con protocolo para visualizar el bulbo olfatorio resultó muy útil para diagnosticar el sitio de las lesiones a la altura de la lámina cribosa del etmoides.