INTRODUCCIÓN
La lactato deshidrogenasa o deshidrogenasa del ácido láctico (LDH) es una enzima presente en múltiples tejidos orgánicos que se libera al plasma como consecuencia de la destrucción celular (fisiológica o patológica). Es un marcador sensible de daño tisular, aunque poco específico para determinar el órgano de origen comprometido1.
La LDH sérica se eleva en numerosas condiciones clínicas, como la hemólisis, cáncer, infecciones graves y sepsis, infarto cerebral, meningitis, encefalitis, infecciones e infartos pulmonares, enfermedades hepáticas, pancreatitis, lesión muscular y miositis, enfermedades hematológicas malignas, infecciones asociadas al virus de la inmunodeficiencia humana, entre muchas otras2, e incluso se la asoció como marcador de mortalidad en pacientes con diabetes hospitalizados por COVID-193. Esta enzima también se eleva por razones preanalíticas, como es la hemólisis in vitro, pudiendo generar resultados falsamente elevados1.
Si bien es posible distinguir 5 isoenzimas de la LDH, que permiten diferenciar hasta cierto punto el órgano o los órganos de procedencia, la determinación de isoenzimas está siendo abandonada de forma progresiva por ser solo relativamente específicas y disponer hoy en día de otros marcadores más eficaces1.
Como un marcador pronóstico y diagnóstico, la LDH sérica elevada por encima del límite superior de la normalidad (alrededor de 100 y 220 U/L, con la reacción en sentido lactato->piruvato)1, fue previamente informada como de mal pronóstico en pacientes con cáncer, incluyendo una variedad de tumores sólidos4,5, en enfermedades hematológicas malignas, así como en pacientes sépticos2. En este mismo sentido, su aumento se asoció en el prediagnóstico de enfermedades malignas con una menor supervivencia global; el riesgo mayor correspondió a aquellos con diagnóstico de cáncer prostático, colorrectal, gastroesofágico, ginecológico y de enfermedades hematológicas malignas6. Por otro lado, en un estudio prospectivo realizado en pacientes sépticos, se llegó a la conclusión de que la mortalidad se encuentra relacionada principalmente con indicadores de disfunción orgánica (Sequential Organ Failure Assessment y Glasgow Scores), el estado nutricional, el ácido láctico, la ferritina y los niveles de LDH7.
Solo se encontraron 2 investigaciones que trabajaron específicamente con poblaciones con LDH extremadamente elevada, aunque con diferentes puntos de corte del biomarcador: la de Erez y cols. (Israel), que evaluó los diagnósticos asociados y el pronóstico de un grupo de pacientes hospitalizados con LDH > 800 U/L, y la de Liu y cols. (China), que analizó la supervivencia global de 311 pacientes con cáncer con LDH mayor de 1000 U/L y una mediana de supervivencia de 1,7 meses2,8.
Si bien un aumento leve o moderado de la LDH sérica en pacientes hospitalizados es muy común, no resulta específica. En contraste, según la investigación de Erez y cols., una LDH sérica aislada y extremadamente elevada (> 800 U/L) podría ser un excelente biomarcador para la presencia de cáncer, metástasis hepáticas, enfermedades hematológicas malignas e infecciones, y un predictor independiente de mortalidad2.
Al evaluar la literatura científica en buscadores de América Latina y el Caribe solo se encontraron artículos sobre el papel pronóstico de la LDH en enfermedades específicas (neumonía por legionella9, infecciones oportunistas en HIV/sida10,11, neumonitis por citomegalovirus (CMV)12, histoplasmosis diseminada grave13, hantavirus14, dengue15,16, preeclampsia17,18, síndrome de hemólisis-elevación de enzimas hepáticas-trombocitopenia (HELLP)19, síndrome urémico hemolítico (SUH)20 y varios tipos de enfermedades oncológicas21-23), pero ningún trabajo global sobre una población de LDH aumentada y mucho menos extremadamente elevada.
En la presente investigación nos proponemos como objetivo analizar la incidencia, diagnósticos asociados y supervivencia global de pacientes adultos con LDH extremadamente elevada (≥ 1000 U/L) de un hospital universitario de la Ciudad Autónoma de Buenos Aires, esclarecer cuáles son los subgrupos de mayor mortalidad según etiología y determinar los factores independientemente asociados a mayor riesgo de fallecimiento. Nuestra hipótesis es que surgirán subgrupos de pacientes dentro de la cohorte que podrían tratarse de pacientes paliativos.
Materiales y métodos
Diseño de estudio, población, criterios de elegibilidad, ámbito y medición de LDH
Cohorte dinámica retrospectiva de la totalidad de pacientes adultos afiliados al plan de salud (PS) de un hospital de alta complejidad de la Ciudad Autónoma de Buenos Aires desde el 01 de enero de 2011 hasta el 31 de diciembre de 2018 inclusive. Los casos fueron identificados como aquellos que presentaron por lo menos un registro de LDH igual a 1000 U/L o mayor, que permitieron calcular la incidencia acumulada anual y la densidad de incidencia de pacientes con este hallazgo de laboratorio durante el período 2011-2018. Se excluyeron como casos aquellos pacientes que presentaron registros de LDH igual a 1000 U/L o mayor previos a la fecha de inicio del estudio, pacientes sin registro previo en la institución pero con antecedente similar en otro centro, y pacientes con un registro de LDH igual a 1000 U/L o mayor, que fueron descartados por presentar alguna situación preanalítica que podría generar resultados erróneos o falsamente alterados (hemólisis in vitro). Se describieron los diagnósticos asociados de los casos y se realizó un análisis de supervivencia de estos. Para el análisis de supervivencia se consideró como punto de partida del seguimiento el primer registro de LDH extremadamente elevado hasta el fallecimiento, la desafiliación o el último contacto (lo que ocurriera primero). Dicha institución es un centro de alta complejidad acreditado por la Joint Commission International, cuyo laboratorio se encuentra acreditado por el Colegio Americano de Patólogos. Hasta octubre de 2012, se realizaron las mediciones de LDH en el autoanalizador Beckman Coulter LX20® en el laboratorio central y CX5® en la sede de la Provincia de Buenos Aires. A partir de esa fecha se comenzaron a utilizar el AU5800® y el AU480®, respectivamente (rango de referencia para LDH para los 4 equipos: 140-280 U/L con la reacción en sentido lactato->piruvato; rango de linealidad para los 4 equipos: 25-14 000 U/L; coeficiente de variación aceptable (CVa) < 5,00%).
Recolección de datos y aspectos éticos
Por medio del sector de Gestión de la Información para la Investigación de la institución, se realizó una revisión sistematizada de las historias clínicas electrónicas de los pacientes que cumplían los criterios de inclusión a partir de un formulario estructurado para tal fin y confeccionado por especialistas en Medicina Interna. El protocolo para la investigación fue evaluado y aprobado previamente a su ejecución por el Comité de Ética de Protocolos de Investigación del centro, cumpliendo con las condiciones éticas establecidas nacional e internacionalmente.
Tamaño muestral y procedimiento de muestreo
A fin de estimar la incidencia acumulada anual de LDH extremadamente elevada en la población, consideramos un tamaño muestral fijo en el período evaluado de aproximadamente 160 000 afiliados adultos al PS. Con este tamaño muestral es posible estimar una incidencia acumulada de por ejemplo 1 en 10 000, con un intervalo de confianza de 95% de entre 0,0253 y 5,57 por cada 10 000 individuos. Esta precisión de la estimación es adecuada para el cálculo de la incidencia acumulada. Debido a que se trata de un hallazgo de baja frecuencia, se incluyeron consecutivamente todos los casos detectados y se utilizaron para el resto de los objetivos.
Análisis estadístico
Se describieron las variables categóricas como frecuencias absolutas y relativas en porcentaje. Se presentaron las variables cuantitativas como media y desvío estándar (DE) o mediana e intervalo intercuartílico según la distribución observada.
Cuando se compararon las características de 2 o más grupos, se evaluó la asociación entre variables con la prueba de Chi Cuadrado, Exacto de Fisher, T, Wilcoxon, Kruskal-Wallis, según supuestos.
Se estimó la incidencia acumulada cruda anual de pacientes adultos del PS con LDH extremadamente elevada entre los años 2011 y 2018, considerando como numerador el número de casos nuevos de LDH extremadamente elevada por año. Se utilizó como denominador el número total de pacientes adultos del PS en riesgo al iniciar cada año. Se calculó el denominador con el número total de pacientes adultos afiliados al PS el 1 de enero de cada año y restando a este valor el número de pacientes con LDH extremadamente elevada diagnosticados años anteriores que sobrevivieron. Todas las incidencias acumuladas se presentan por cada 10 000 individuos con sus intervalos de confianza de 95% (IC 95%) calculados con el método exacto.
Se estimó la densidad de incidencia cruda de pacientes adultos con LDH extremadamente elevada del PS en el período 2011-2018. Se presentaron adicionalmente las incidencias específicas para el sexo masculino, femenino y por grupos etarios. Se estandarizaron las tasas utilizando el estándar propuesto por la Organización Mundial de la Salud (OMS)24 y la población argentina según el censo 201025 por sexo y edad con el método directo. El numerador estuvo representado por la cantidad de casos de pacientes con, por lo menos, un registro de LDH o igual a 1000 U/L o mayor. El denominador estuvo representado por la suma del tiempo en riesgo en personas/año de todos los pacientes adultos del padrón de afiliados. Todas las densidades de incidencia se presentaron por cada 10 000 personas año con sus respectivos IC 95%.
Se estimó la mortalidad de los pacientes con LDH ≥ 1000 U/L en función del tiempo con el método de Kaplan-Meier. Se presentaron las curvas de supervivencia según etiología y la supervivencia estimada al mes, 2, 3, 6 y 12 meses, con sus intervalos de confianza (IC 95%), de todos los pacientes con la condición y según etiología. Se calculó la mediana de supervivencia en todos los pacientes con LDH extremadamente elevada y según etiología. Se compararon las curvas de supervivencia con la prueba de Cox-Mantel de acuerdo con la etiología. Para las variables categóricas politómicas se realizaron comparaciones múltiples en las que se obtuvieron los p valores ajustados multiplicando los p valores por el número de comparaciones, de acuerdo con el método propuesto por Bonferroni.
Se utilizó un modelo de regresión de riesgos proporcionales de Cox para estimar los hazard ratios (HR) crudos y ajustados, que incluyeron las variables edad, sexo, rango de LDH, año de diagnóstico y etiología. Se evaluó el supuesto de proporcionalidad en cada análisis bivariado basado en residuos de Shoenfeld y evaluación gráfica. Se presentaron los HR con sus IC 95%.
Se consideraron estadísticamente significativas las probabilidades menores del 5%.
El análisis estadístico se realizó con el software STATA versión 15® (StataCorp. 2017. Stata Statistical Software: Release 15. College Station, TX: StataCorp LLC).
Resultados
Durante el período evaluado se registraron 542 pacientes mayores de 18 años con al menos un valor de LDH igual a 1000 U/L o mayor. Se excluyeron 20 pacientes (3,69%) debido a una condición preanalítica de la muestra, por lo que finalmente se incluyeron 522 casos (96,31%) para el análisis.
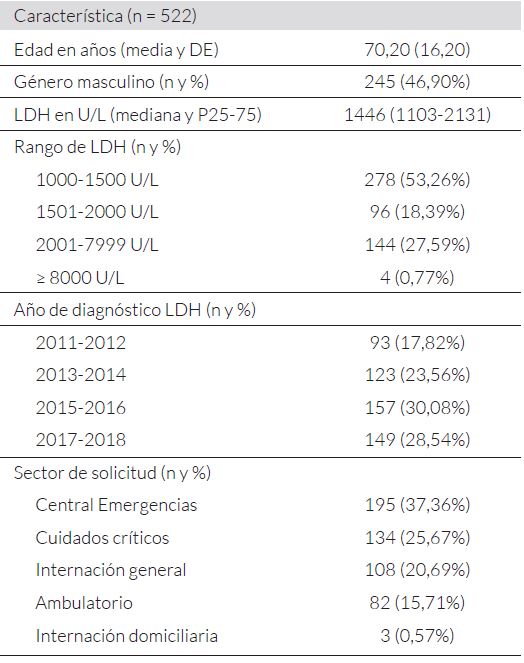
En la tabla 1 se describen las características basales y clínicas de los pacientes con LDH ≥ 1000 U/L. La media de edad fue de 70,20 años (DE 16,20), el 53,10% eran mujeres y la mediana de LDH fue de 1446 U/L (P25% 1103 U/L-P75% 2131 U/L). La mayor parte de los registros se tomaron a partir de solicitudes desde la central de emergencias de adultos, lo que representa el 37,36%.
Tabla 1. Características de los pacientes con LDH ≥ 1000 U/L
Incidencia acumulada anual de pacientes con LDH extremadamente elevada
En el primer año del período de seguimiento (2011), por cada 10 000 pacientes del Plan de Salud, 3,31 pacientes (IC 95%: 2,39-4,48) presentaron por lo menos un registro de LDH extremadamente elevada (42 casos y 126 767 pacientes en riesgo); mientras que en el último año de estudio (2018), por cada 10 000 pacientes, lo presentaron 4,93 (IC 95%: 3,90-6,20) (73 casos y 148 001 pacientes en riesgo). En el período de seguimiento, la menor incidencia acumulada se registró en el año 2011, mientras que la mayor se registró en 2016, con 6,1 pacientes (IC 95%: 4,85-7,47) cada 10 000 (87 casos y 143 631 pacientes en riesgo).
Densidad de incidencia de pacientes con LDH extremadamente elevada en el período 2011-2018
La densidad de incidencia cruda de pacientes adultos con LDH extremadamente elevada del Plan de Salud en el período 2011-2018 fue de 4,63 (IC 95%: 4,25-5,04) por cada 10 000 personas/año, mientras que la densidad de incidencia específica en hombres fue de 5,44 (IC 95%: 4,80- 6,17) y en mujeres de 4,09 (IC 95%: 3,64-4,60). La densidad de incidencia específica aumentó progresivamente con la edad, mientras que entre los 20 y 30 años fue de 0,86 (IC 95%: 0,46-1,61), en mayores de 80 años fue de 11,51 (IC 95%: 9,93-13,33). Las tasas estandarizadas por edad y sexo (WHO y Argentina según el censo 2010) fueron 2,25 (IC 95%: 1,62-2,88) y 2,39 (IC 95%: 1,75-3,02), respectivamente.
Etiologías
En la tabla 2 se describen las etiologías discriminadas por grupo que explicaron potencialmente los registros de LDH extremadamente elevados de los pacientes.
Tabla 2. Discriminación de las etiologías de pacientes con LDH extremadamente elevada

*1 caso de anemia hemolítica por válvula protésica, 1 caso de enfermedad de Still del adulto, 1 caso de síndrome hemofagocítico, 1 caso de status epiléptico y 1 caso de pancreatitis.
El 96,20% de los pacientes con enfermedades oncológicas sólidas presentaban metástasis al momento de dar a conocer el primer registro de LDH ≥ 1000 U/L. El estado funcional de los pacientes con enfermedades oncológicas sólidas versus los pacientes con enfermedades oncohematológicas al momento de presentar el primer registro de LDH extremadamente elevada fue distinto en forma estadísticamente significativa (p valor < 0,001), con un estado funcional 3-4 del 44,94% versus 22,12%, respectivamente.
Análisis de supervivencia de pacientes con LDH ≥ 1000 U/L (global y por etiología)
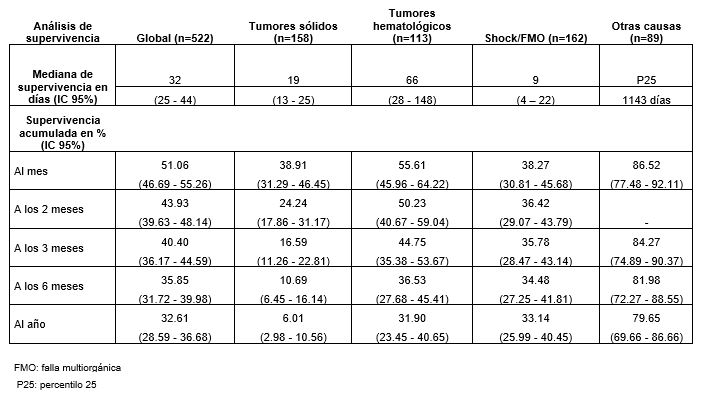
En la tabla 3 se observa la mediana de supervivencia y la supervivencia acumulada al mes, a los 2, 3, 6 y 12 meses del total de pacientes con LDH extremadamente elevada, y discriminado por etiología (análisis univariado). Se destacó la curva de supervivencia de los pacientes con enfermedades oncológicas sólidas, que presentaron mayor mortalidad en el transcurso del primer año de seguimiento.
Tabla 3. Análisis de supervivencia de pacientes con LDH extremadamente elevada global y por etiología
Se observaron diferencias estadísticamente significativas entre la supervivencia de los pacientes con enfermedades oncológicas sólidas, oncohematológicas, no oncológicas con shock/FMO, y no oncológicas no shock/FMO (p < 0,001). Al realizar comparaciones múltiples entre las curvas de supervivencia por etiología, los pacientes con enfermedades oncológicas sólidas y oncohematológicas presentaron un comportamiento significativamente distinto, con una mayor mortalidad a favor de los primeros (p < 0,001), al igual que los pacientes con enfermedades no oncológicas no shock/FMO con el resto de las categorías (p < 0,001).
El gráfico de Kaplan-Meier de los pacientes con LDH extremadamente elevada por etiología se observa en la figura 1.
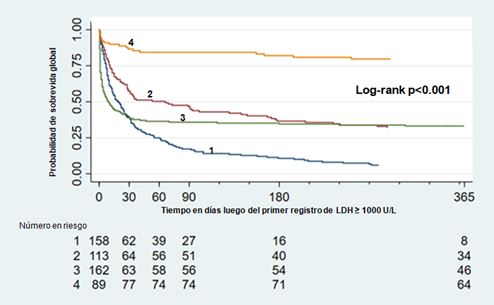
Figura 1. Gráfico de Kaplan-Meier de las curvas de supervivencia estimadas de los pacientes con LDH extremadamente elevada por subgrupos de etiología.
1: pacientes con enfermedades oncológicas sólidas; 2: pacientes con tumores hematológicos; 3: pacientes con shock/fallo multiorgánico de cualquier origen; 4: pacientes con otras causas.
En la escala vertical, las cifras con decimales deben llevar comas, no puntos: 0,00,0,025, etc.
Factores asociados a mortalidad
Las variables sexo, edad, rango de LDH, año de diagnóstico (para analizar indirectamente el avance en tecnologías sanitarias) y etiología se asociaron en forma estadísticamente significativa a mortalidad tanto en el análisis bivariado como en el análisis multivariado (Tabla 4). El modelo de regresión múltiple pone de manifiesto que la etiología es la variable explicativa asociada a mortalidad de mayor peso, destacándose la categoría de pacientes con enfermedades oncológicas sólidas como los de mayor riesgo.
Tabla 4. Factores asociados a mortalidad en pacientes con LDH extremadamente elevada. Análisis bivariado y multivariado
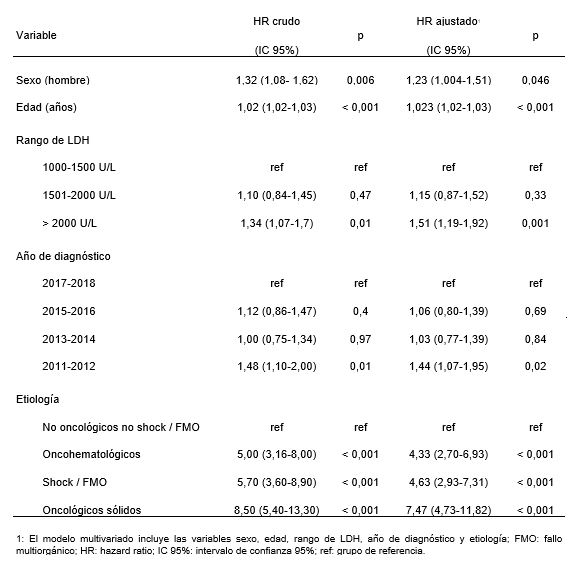
1: El modelo multivariado incluye las variables sexo, edad, rango de LDH, año de diagnóstico y etiología; FMO: fallo multiorgánico; HR: hazard ratio; IC 95%: intervalo de confianza 95%; ref: grupo de referencia
Análisis de supervivencia de pacientes con enfermedades oncológicas sólidas tratados vs. no tratados, luego de presentar el primer registro de LDH extremadamente elevada
De 158 pacientes con enfermedades oncológicas sólidas de la muestra, luego de presentar el primer registro de LDH extremadamente elevada, 116 pacientes (73,42%) no recibieron tratamiento oncoespecífico, mientras que 42 pacientes (26,58%) sí lo hicieron. La mediana de supervivencia y la supervivencia acumulada al año de los pacientes no tratados fue de 12 días (IC 95%: 9-16 días) y del 2,09% (IC 95%: 0,43-6,43), respectivamente. Por su parte, el mismo análisis en los pacientes tratados resultó ser de 69 días (IC 95%: 47-130 días) y 16,67% (IC 95%: 7,33-29,27), respectivamente. Se observaron diferencias estadísticamente significativas en la supervivencia de ambos grupos (p < 0,001). La única variable que fue significativamente distinta entre los grupos fue el estado funcional (p < 0,01): los pacientes no tratados presentaron mayor porcentaje de estado funcional 3-4 (no tratados 70% vs. tratados 44,4%).
Discusión
Según nuestro conocimiento, este es el primer trabajo de investigación que describe la incidencia de pacientes con LDH extremadamente elevada, por lo cual resulta novedoso.
Los resultados apoyan lo previamente expuesto por el trabajo de Erez y cols., que consideran a la LDH sérica aislada y extremadamente elevada (> 800 U/L) como un marcador de un grupo muy específico de enfermedades graves, a diferencia del aumento leve o moderado que es muy común en pacientes hospitalizados, pero poco específico2. De los 522 pacientes con LDH extremadamente elevada analizados en nuestra investigación, 433 (83%) presentaron enfermedades oncológicas o shock/fallo multiorgánico de cualquier etiología. A diferencia del trabajo antes mencionado que enfatiza que la mayoría de las causas eran cáncer avanzado e infecciones graves2, a nosotros nos gustaría remarcar que ‒además de enfermedades oncológicas sólidas y oncohematológicas‒ el shock o fallo multiorgánico de cualquier origen es el que se relaciona con la LDH extremadamente elevada, y no solo las infecciones graves. Una ventaja de la investigación de Erez y cols. es que contó con un grupo control que mostró una mortalidad intrahospitalaria de estos pacientes del 26,6% contra el 4,3% sin esta condición. Nuestra investigación no contó con un grupo control, pero tuvo el beneficio de evaluar desenlaces a largo plazo e incorporar la perspectiva de cuidados paliativos en algunos subgrupos de pacientes.
En lo que respecta a la mortalidad según etiología en pacientes con LDH sérica extremadamente elevada, encontramos diferencias estadísticamente significativas entre ellas. Vale la pena remarcar la importancia de haber separado el análisis de los pacientes oncológicos sólidos y oncohematológicos, no realizado con tanta profundidad en otros trabajos similares. Sosteníamos la hipótesis de que la supervivencia en estos subgrupos sería distinta, situación que terminamos respaldando con nuestros resultados (p < 0,001). Liu y cols. estimaron una mediana de supervivencia de 1,7 meses y una supervivencia acumulada al año del 15,6% para todos los pacientes oncológicos con LDH > 1000 U/L8. En nuestra cohorte, los pacientes oncológicos sólidos presentaron una mediana de supervivencia de 0,63 meses y una supervivencia acumulada al año del 6,01%, mientras que los pacientes oncohematológicos presentaron una mediana de supervivencia de 2,2 meses con una supervivencia acumulada del 31,90% en el mismo período. Esto sugiere un mejor pronóstico a corto y largo plazo y una menor velocidad de ocurrencia del evento en los últimos.
Entre las etiologías se destacan los pacientes con enfermedades oncológicas sólidas como aquellos de peor pronóstico; puede tratarse de pacientes candidatos a realizar un seguimiento por cuidados paliativos y suspender tratamientos oncoespecíficos. No podemos decir con certeza si un pequeño subgrupo de pacientes podría beneficiarse con tratamientos. La investigación de Liu y cols. encuentra un pequeño porcentaje de pacientes con estado funcional 1-2 y con disminución de los registros de LDH a los 2 meses de tratamiento con un posible beneficio, pero no subdivide en forma clara a los pacientes con enfermedades oncohematológicas y enfermedades oncológicas sólidas8. Para sacar conclusiones definitivas acerca del papel del tratamiento en esta población, sería necesario considerar otras variables de confusión y un diseño de estudio más apropiado para explorar esta hipótesis.
El papel pronóstico de la LDH sérica en oncología ha sido reconocido por mucho tiempo. La LDH es una enzima clave en el proceso de producción de energía en las células cancerosas: cataliza la conversión de piruvato a lactato en condiciones hipóxicas26. Debido a su función en el metabolismo anaeróbico, las células cancerosas crecen incluso después de su rápida proliferación que conduce a condiciones de bajo oxígeno en el microambiente tumoral27. Por lo tanto, la LDH desempeña un papel importante en la progresión y mantenimiento del tumor, y ha sido considerada como blanco terapéutico28,29. Los niveles de LDH aumentan en respuesta a la lesión del tejido y dependiendo del estadio de enfermedad, y podría ser un marcador de carga tumoral para pacientes con cáncer avanzado30. Un nivel más alto de LDH se relacionó con una supervivencia más corta en varios tipos de cáncer26.
Los pacientes con shock o fallo multiorgánico de cualquier origen presentaron, llamativamente, la mediana de supervivencia más baja de todas las etiologías, 9 días, lo que demuestra una gran velocidad inicial en la ocurrencia del evento. Aparentemente estos pacientes tuvieron un comportamiento a “todo o nada” durante el primer mes, para luego estabilizarse, demostrado en la supervivencia acumulada a los 30 días del 38,27% y al año del 33,14%.
Por último, los pacientes no oncológicos distintos de shock y fallo multiorgánico, presentaron un comportamiento en la supervivencia estadísticamente diferente del resto de las etiologías y fueron los de mejor pronóstico, con una supervivencia acumulada al año del 79,65%.
La edad, el sexo masculino, el diagnóstico de enfermedad oncológica sólida, el diagnóstico de enfermedad oncohematológica, el diagnóstico de shock y/o FMO de cualquier etiología, un rango de LDH mayor de 2000 U/L y el diagnóstico de la LDH extrema durante los años 2011-2012 se asociaron independientemente a mayor riesgo de muerte en el período de seguimiento del estudio.
Como debilidades de nuestra investigación se puede decir que, en primer lugar, se trató de un estudio unicéntrico y podría no ser representativo de la población de esta ciudad. Además, el tamaño muestral es relativamente bajo para justificar el efecto de múltiples características clínicas en la supervivencia y es insuficiente para realizar análisis de subgrupo. Por otro lado, este trabajo analiza una cohorte retrospectiva y algunos datos fueron más difíciles de recabar. Finalmente, no identificamos qué pacientes persistieron con LDH extremadamente elevada y en quiénes disminuyó o se normalizó luego del primer registro, una variable manifestada por otros trabajos como asociada a mortalidad.
A su vez, encontramos fortalezas. Para empezar, trabajar con una población cerrada tiene como ventaja baja pérdida de seguimiento y como consecuencia una mejor estimación de la mortalidad. Por otro lado, la historia clínica electrónica aseguró la correcta detección de los pacientes en cuestión, la calidad del registro médico y el nivel de control de la información ingresada.
Conclusión
El solo hecho de que los pacientes presenten un registro de LDH sérica extremadamente elevada aportaría una valiosa información a los médicos tratantes desde el punto de vista diagnóstico y pronóstico.
En los pacientes con enfermedades oncológicas sólidas, un registro sérico de LDH extremadamente elevado podría considerarse un biomarcador de terminalidad, teniendo en cuenta el inicio de cuidados paliativos y la suspensión de tratamientos oncoespecíficos.
Se requieren nuevas investigaciones con diseños que incluyan un grupo control para confirmar estas hipótesis.