RESUMEN
Introducción
Imaginemos la posibilidad de realizar un diagnóstico etiológico certero, casi semejante al resultado anatomopatológico, pero con nuestros propios ojos. Así se introdujo el término biopsia óptica, en referencia a la precisión diagnóstica del filtro de luz de banda estrecha o narrow band imaging (NBI) al evaluar lesiones de la mucosa aerodigestiva superior. La morbimortalidad del cáncer de laringe disminuye al detectar y tratar el tumor de forma temprana. Nuestro objetivo es analizar los resultados obtenidos sobre sensibilidad y especificidad del filtro NBI para la detección de lesiones laríngeas tempranas en los trabajos publicados entre 2011 y 2021. Como objetivos secundarios evaluaremos el papel del NBI en el intraoperatorio y las clasificaciones validadas para la aplicación de esta tecnología.
Estado del arte
La media de sensibilidad del NBI hallada para lesiones premalignas en este análisis fue de 88% en comparación con luz blanca o white light (WL) solo que fue de 78,4%. La media de especificidad fue de 81,4% en comparación con WL pero resultó de 68,7%. La variación de sensibilidad de NBI vs. WL fue de 13,8% y de especificidad fue de 13,6%. Con respecto a la evaluación luego de tratamiento quimiorradiante, Piazza y cols. establecen que el NBI permite un 20% más de detección de persistencias o recurrencias por sobre las endoscopias clásicas.
Discusión
El Narrow Band Imaging (NBI) mejora significativamente la detección temprana de lesiones malignas y recidivas en la laringe, superando la sensibilidad de la luz blanca convencional. Su uso sistemático optimiza la interpretación diagnóstica, reduce biopsias innecesarias y mejora la delimitación de márgenes quirúrgicos, incluso en procedimientos en consultorio. Aunque no reemplaza al estudio histopatológico, el NBI constituye una herramienta clave que incrementa la precisión diagnóstica y la seguridad oncológica. Existen dos clasificaciones validadas, la de Ni y la de la European Laryngological Society (ELS).
Conclusión
El NBI se consolida como una herramienta esencial para la detección temprana y la evaluación precisa de lesiones laríngeas, mejorando la seguridad diagnóstica y quirúrgica. Aunque no sustituye al estudio histopatológico, potencia significativamente la toma de decisiones clínicas y reduce procedimientos invasivos.
Palabras clave: Luz de banda estrecha, cáncer laríngeo temprano, endoscopia laríngea.
Narrowband imaging (NBI): a literature review of its usefulness in laryngology
ABSTRACT
Introduction
Imagine the possibility of achieving an accurate etiological diagnosis, almost comparable to the histopathological result, but with our own eyes. This is how the term optical biopsy was introduced, referring to the diagnostic precision of the narrow band imaging (NBI) light filter when assessing lesions of the upper aerodigestive mucosa. The morbidity and mortality of laryngeal cancer decrease when the tumor is detected and treated early. Our objective is to analyze the results obtained regarding the sensitivity and specificity of the NBI filter for detecting early laryngeal lesions in studies published between 2011 and 2021. As secondary objectives, we will assess the role of NBI in the intraoperative setting and the validated classifications for applying this technology.
State of the art
The mean sensitivity of the NBI found for premalignant lesions in this analysis was 88% compared to white light (WL), which was 78.4%. The mean specificity was 81.4% compared to WL, which was 68.7%. The variation in sensitivity of NBI vs. WL was 13.8% and specificity was 13.6%. Regarding the evaluation after chemoradiation treatment, Piazza et al. establish that NBI allows 20% more detection of persistence or recurrence than classic endoscopies.
Discussion
Narrow Band Imaging (NBI) significantly enhances the early detection of malignant and recurrent laryngeal lesions, surpassing the sensitivity of conventional white light. Its systematic use optimizes diagnostic interpretation, reduces unnecessary biopsies, and improves surgical margin delineation, even in in-office procedures. Although it does not replace histopathological evaluation, NBI is a key tool that increases diagnostic accuracy and oncologic safety. Two validated classifications exist: the Ni classification and that of the European Laryngological Society (ELS).
Conclusion
NBI is established as an essential tool for the early detection and accurate assessment of laryngeal lesions, improving both diagnostic and surgical safety. Although it does not replace histopathological analysis, it significantly enhances clinical decision-making and reduces invasive procedures.
Key words: Narrow band imaging, early laryngeal cancer, laryngeal endoscopy.
INTRODUCCIÓN
El cáncer de laringe tiene una incidencia del 2% y una mortalidad del 1% en la población general mundial sin distinguir por edad y sexo, según los informes de la Organización Mundial de la Salud en 2020. El síntoma cardinal que hace sospechar su presencia es la disfonía, sobre todo en los cánceres glóticos (GLOBOCAN 2020 - International Agency for Research on Cancer 2024).
Los principales factores de riesgo son el tabaquismo y el alcoholismo. La relación sinérgica entre el alcohol y el tabaco se reconoce desde 1990, lo que ha contribuido al aumento del conocimiento sobre la etiología del cáncer laríngeo. En los últimos años se ha observado una disminución en la incidencia de este tipo de cáncer, posiblemente debido a una mayor conciencia sobre los peligros del consumo de tabaco y a las campañas antitabaco1,2.
Los carcinomas de células escamosas, que constituyen la mayoría de los casos de cáncer de laringe, pueden presentarse en cualquier área de la cabeza y el cuello. Estos tumores tienen la característica de poder manifestarse en otros sitios de forma sincrónica o metacrónica3.
La detección temprana de los tumores de laringe mejora significativamente la sobrevida y la calidad de vida de los pacientes. Según datos de la Asociación Americana de Cáncer, la tasa de supervivencia a cinco años de los carcinomas glóticos localizados es del 84%, mientras que para los tumores supraglóticos y subglóticos la supervivencia es del 61% y 59%, respectivamente. En contraste, para los tumores avanzados, la supervivencia a cinco años disminuye considerablemente, 45% para los glóticos, 30% para los supraglóticos y 44% para los subglóticos4.
La detección temprana permite, además, tratar estos tumores con técnicas menos invasivas, como la microcirugía transoral de laringe. Este tipo de intervenciones, si bien se realizan en el quirófano y bajo anestesia general, son menos invasivas que la cirugía convencional, se pueden realizar de forma ambulatoria y conllevan una baja morbilidad. De lo contrario, cuando los tumores son más avanzados o se han diseminado a otras áreas, el tratamiento quirúrgico incluye la extirpación parcial o total del órgano y sus estaciones ganglionares. Estos procedimientos implican una mayor morbilidad, como disfagia o la necesidad de traqueostomía, y suelen requerir hospitalización prolongada.
El diagnóstico de cáncer de laringe se basa en estudios endoscópicos e imagenológicos. La tomografía computarizada (TC) y la resonancia magnética (RM) son las técnicas de imágenes más comunes. Algunos estudios sugieren que la resonancia es más sensible para lesiones unilaterales y la tomografía es más útil en casos bilaterales, especialmente para detectar compromiso extralaríngeo5.
Para evaluar la anatomía y función laríngea disponemos de múltiples métodos de diagnóstico endoscópico, entre ellos la laringoscopia indirecta, la videoendoscopia con fibra flexible u óptica rígida con luz continua o luz estroboscópica.
En el mundo, desde el año 1995, la rinofibrolaringoscopia forma parte del examen físico otorrinolaringológico en la búsqueda de cánceres de mucosa aerodigestiva superior. La luz usada en este estudio es la luz blanca convencional (white light - WL).
La luz de imagen de banda estrecha (narrow band imaging - NBI) es una tecnología moderna que aprovecha las características del espectro de luz para identificar con mayor precisión la vascularización y el patrón vascular presente en una superficie mucosa (Fig. 1). De esta forma brinda mayor orientación en lesiones sospechosas de malignidad por la neoangiogénesis tumoral. Inicialmente, el NBI se usó para identificar tumores gastrointestinales; luego su uso se extendió a hipofaringe y orofaringe. Actualmente, también para estudiar tumores tempranos laríngeos6.
Asimismo, es importante disminuir la variabilidad interobservador a través de clasificaciones que sistematizan el análisis de las imágenes obtenidas; resulta especialmente útil para los otorrinolaringólogos o cirujanos de cabeza y cuello con poca experiencia.
Independientemente del subsitio tumoral de la cabeza y el cuello, el NBI es útil para la detección de los cánceres tempranos, pesquisa y seguimiento posterior a quimioterapia o radioterapia e incluso intraoperatoriamente para delimitar la seguridad de los márgenes quirúrgicos.
Piazza y cols.7 introducen el concepto de optical biopsy o biopsia óptica para las técnicas de endoscopia biológica que proporcionan una visión profunda del comportamiento de una lesión en estudio y permiten la visualización de lesiones que, sin la implementación de este método, podrían no detectarse. Si bien, el estudio anatomopatológico sigue siendo el procedimiento de referencia (patrón de oro) del diagnóstico de estas lesiones, la endoscopia biológica tiene como fin disminuir el número de biopsias innecesarias y los falsos negativos, ayudando a elegir el sitio para biopsiar7,8.
En la bibliografía se describe un 18% más de detección de carcinomas laríngeos con el uso del NBI en comparación con la luz blanca clásica, incluso en pacientes que recibieron tratamiento radiante o quimiorradiante9.
OBJETIVO
El objetivo de este trabajo es conocer los beneficios y resultados de sensibilidad y especificidad del uso sistemático del NBI en la evaluación de lesiones laríngeas y comparar sus resultados con los de la luz blanca (white light). Como objetivos secundarios, buscamos detallar los beneficios de su uso sistemático en el ámbito intraoperatorio, sobre todo en la determinación de los márgenes oncológicos de resección y, por último, conocer las clasificaciones validadas de lesiones estudiadas por NBI.
ESTADO DEL ARTE
Estrategia de búsqueda
Se realizó una búsqueda bibliográfica de trabajos publicados con la celdilla de búsqueda: (LaryngealNeoplasms/ diagnosis [Majr]) AND Narrow Band Imaging [Majr] en la base de datos PubMed. Se hallaron 42 trabajos publicados en total, desde el año 2009 hasta el año 2021.
En la base de datos BVSalud se utilizó la celdilla de búsqueda: (mh:(Neoplasias Laríngeas/DI) AND narrow band imaging). Se hallaron 31 trabajos publicados desde el año 2010 hasta el año 2021.
Criterios de inclusión y exclusión
Se incluyeron trabajos en idioma inglés o español, referidos a lesiones neoplásicas tempranas de laringe que hayan sido evaluadas con el filtro de luz NBI para su diagnóstico o para su tratamiento intraoperatorio.
Se excluyeron trabajos en otros idiomas, trabajos que tuvieran como objetivo la evaluación de lesiones benignas (por ejemplo, papilomatosis laríngea), trabajos que se enfocaran en otras tecnologías o inteligencia artificial distintas del NBI.
Extracción de datos
Los autores extrajeron la siguiente información: primer autor, año de publicación, origen, cantidad de pacientes incluidos en el análisis, duración del estudio, sensibilidad y especificidad de las técnicas utilizadas (WL y NBI).
Luego de la revisión se obtuvo un total de 73 trabajos. Se descartaron 7 trabajos por duplicidad. De los 66 trabajos restantes se excluyeron 45 (14 por encontrarse en otro idioma distinto de inglés o español y 31 por centrarse en otras patologías, tecnologías o información incompleta).
En total se analizaron 21 trabajos publicados entre los años 2009 y 2021 (15 de la base de datos PubMed® y 6 de la base de datos BVSalud®). Se registró un resumen de todos los trabajos en la tabla 1.
Con respecto al método para la aplicación del NBI se formaron dos grupos: uno que se enfocó en realizar el estudio en pacientes ambulatorios y otro que realizó la endoscopia en el ámbito intraoperatorio. En el primer grupo, todos los trabajos establecieron que debería realizarse en posición de sedestación bajo anestesia local por vía nasal con lidocaína.
El segundo grupo usó el NBI en el quirófano inmediatamente después de la intubación para delimitar las lesiones.

Figura 1. En esta imagen se puede apreciar la penetración de las distintas longitudes de onda de la luz. En el caso de 415 nm - azul, alcanza hasta los capilares de la mucosa y emite luz marrón. En caso de 540 nm - verde, hasta las venas submucosas y emite luz azul cyan - (Figura tomada de Lukes P, y col.5)
1. Sensibilidad y especificidad del NBI en la detección de lesiones premalignas y malignas de laringe
En 2009, Watanabe y cols. 9 realizaron un estudio de 35 pacientes, encontrando una sensibilidad de 91,3% y especificidad de 91,6% al utilizar el NBI en lesiones laríngeas sospechosas. Piazza y cols.10, en 2010, evaluaron 279 pacientes, e informaron una sensibilidad general de 98% y especificidad de 90%, pero con una sensibilidad de solo 60% en lesiones premalignas en su grupo de pacientes en seguimiento. Irjala y cols. 3, en 2011, obtuvieron una sensibilidad de 55% y especificidad de 98% para lesiones malignas en su cohorte, destacando que el NBI resultó útil en pacientes con antecedentes de cáncer laríngeo.
Ni y cols.11, en 2011, con 85 pacientes, encontraron una sensibilidad de 88,9 % en la detección de lesiones malignas usando NBI, en comparación con 68,9% mediante WL.
Otros estudios, como el de De Vito y cols. 12, informaron una alta sensibilidad (97%) y especificidad (92,5%) al usar el NBI, pero sin diferencias estadísticamente significativas con respecto a la clasificación de Ni. Por su parte, Rzepakowska y cols.13, en 2018, estudiaron 62 pacientes, encontrando una especificidad de 97,4% y sensibilidad de 100% para lesiones malignas. Lin y cols. 14, en 2021, observaron una alta sensibilidad para lesiones benignas (90,91%) y malignas (93,51%) al utilizar NBI, pero una sensibilidad baja para lesiones premalignas (41,67%).
2. Comparación WL vs. NBI
Piazza y cols.15, en 2010, demostraron que el NBI incrementó la sensibilidad con respecto a WL (100% frente a 66%), sin modificar la especificidad (98% frente a 100%, respectivamente). En 2019, Ni y cols.16 encontraron que la capacitación mejoraba la especificidad del NBI, aumentando de 64 a 75% tras un curso de formación.
Shoffel-Havakuk y cols.17, en 2016, también observaron un incremento en la sensibilidad usando NBI, pero la especificidad fue más baja en comparación con WL. En 2016, Ni y cols. 18 compararon NBI, WL y autofluorescencia (AF), y encontraron que NBI era superior a WL en términos de especificidad (85% frente a 48%). Bäck y cols. 19 informaron, en 2017, una sensibilidad de 100% con NBI frente a 62% con WL. Sakthivel y cols.20, en 2018, observaron un aumento en la sensibilidad al usar NBI combinado con WL, alcanzando un 100%. Popek y cols.21, en 2019, también hallaron una mayor sensibilidad (98,5%) y especificidad (98,5%) con NBI en comparación con WL.
Zwakenberg y cols.22, en 2021, demostraron que el NBI con fibra flexible tuvo una sensibilidad comparable a la de la laringoscopia rígida, destacando su utilidad en la evaluación de lesiones en consultorio.
3. Uso de NBI intraoperatorio
Garofolo et al. 23, en 2015, destacaron que el NBI intraoperatorio redujo significativamente los márgenes positivos (23,7% con WL frente a 3,6% con NBI). Klimza y cols. 24, en 2018, con 44 pacientes, refirieron una sensibilidad de 100% con NBI en comparación con 79,5% con WL. Rzepakowska y cols. 25, en 2018, encontraron que el NBI incrementó la sensibilidad para lesiones premalignas (98,8%) y malignas (97,6%) con respecto a WL (90,2% y 92,9%, respectivamente).
4. Uso del NBI después de radioterapia/ quimiorradioterapia
En 2010, Piazza y cols.15 concluyeron que el NBI es altamente sensible (100%) y específico (98%) para detectar recurrencias en pacientes posteriores a radioterapia y quimiorradioterapia, demostrando un 20% más de detección en comparación con WL. El NBI permite diferenciar entre efectos inflamatorios y neoplasias activas, lo que lo convierte en una herramienta valiosa en el seguimiento posterior al tratamiento.
5. Validación de la clasificación endoscópica de las lesiones evaluadas con NBI
Bertino y cols.26, en 2015, al aplicar la clasificación de Ni (Fig. 2), encontraron que el uso de NBI aumentó significativamente la especificidad (84,6%) y el valor predictivo positivo (91,6%) en comparación con WL, con una sensibilidad de 98,1% similar a la de otros estudios.
6. Aporte de la luz estroboscópica a la WL+ NBI
En 2017, Yang y cols. 27 demostraron que la combinación de luz estroboscópica con WL y NBI mejora la especificidad y el valor predictivo positivo en la evaluación de lesiones laríngeas, con una mejora estadísticamente significativa en comparación con el uso solo deWL y NBI.
7. Validación interobservador e intraobservador del uso del NBI vs. WL
Davaris y cols.28, en 2019, refirieron una mayor fiabilidad interobservador con NBI (kappa=0.849) en comparación con WL (kappa=0.661), aunque la fiabilidad intraobservador fue similar entre ambos métodos.
8. Limitaciones halladas en el uso del NBI
Rzepakowska y cols.26 señalaron que el engrosamiento epitelial en algunas leucoplasias dificulta la evaluación con NBI, así como la confusión entre lesiones papilomatosas y carcinoma bien diferenciado es otra limitación.
Por otro lado, el NBI no permite determinar la profundidad de la infiltración tumoral, siendo necesario siempre realizar biopsias para obtener esta información.
Zwakenberg y cols. 22 mencionaron que las lesiones sangrantes pueden interferir la fiabilidad del NBI debido a la absorción de luz por la hemoglobina, lo que produce patrones de captación poco claros.
La curva de aprendizaje también fue mencionada como una limitación, ya que la interpretación adecuada del NBI requiere práctica y capacitación, lo que puede aumentar inicialmente la tasa de falsos positivos.
Tabla 1. Características del análisis.
| N | DOI | Título | País | Año | Primer autor | Seguimiento | Muestra | Sensibilidad NBI | Especificidad NBI |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 10.1007/s00405-008-0835-1 | The value of narrow band imaging for early detection of laryngeal cancer | Japón | 2009 | Watanabe et al. | 14 meses | 35 | 91,3% | 91,6% |
| 2 | 10.1007/s00405-010-1236-9 | Role of narrow-band imaging and HDTV in surveillance after chemo/radiotherapy | Italia | 2010 | Piazza et al. | 24 meses | 59 | 100%I | 98%I |
| 3 | 10.1007/s00405-009-1121-6 | Narrow band imaging and HDTV in the assessment of laryngeal cancer | Italia | 2010 | Piazza et al. | 18 meses | 279 | 60% (98% NBI+HDTV) | 87% (90% NBI+HDTV) |
| 4 | 10.1007/s00405-011-1516-z | Pharyngo-laryngeal examination with NBI: early experience | Bélgica | 2011 | Irjala et al. | 18 meses | 73 | 55% | 98% |
| 5 | 10.1017/S0022215110002033 | Endoscopic diagnosis of laryngeal cancer and precancerous lesions by NBI | China | 2011 | Ni et al. | 6 meses | 85 | 88,9% (68,9% WL)II | 93,2% (89,8% WL) |
| 6 | 10.1002/hed.23582 | Effectiveness of NBI in premalignant and malignant laryngeal lesions | Italia | 2015 | Bertino et al. | 24 meses | 248 lesiones (217 pacientes) |
97,4% (98,1%)III | 84,6% (56%)III |
| 7 | 10.1177/0003489414556082 | Intraoperative NBI during transoral laser microsurgery | Italia | 2015 | Garofolo et al. | 21 meses | 82 | No dataIV | |
| 8 | 10.1111/coa.12728 | NBI as screening test for early detection of laryngeal cancer | Italia | 2016 | De Vito et al. | 48 meses | 73 | 97% | 92,5% |
| 9 | 10.1002/lary.26263 | Does NBI improve preoperative detection of glottic malignancy? | Israel | 2016 | Shoffel-Havakuk et al. | 24 meses | 45 lesiones (36 pacientes) |
58,6% (48,7% WL) | 61,2% (76,1% WL) |
| 10 | 10.1017/S0022215116009002 | NBI versus autofluorescence imaging | China | 2016 | Ni et al. | 6 meses | 65 lesiones (50 pacientes) |
95% (74% WL) | 85% (67% WL) |
| 11 | 10.1002/lary.26526 | Feasibility of NBI in suspected upper airway lesions | Finlandia | 2017 | Back et al. | 8 semanas | 125 | 100% WL (62%) | 84% (WL 81%) |
| 12 | 10.1080/00016489.2017.1388542 | NBI combined with stroboscopy | China | 2017 | Yang et al. | 45 meses | 160 lesiones (110 pacientes) |
67% | 72% |
| 13 | 10.1016/j.bjorl.2018.01.004 | Intraoperative NBI in transoral laser microsurgery | Italia | 2018 | Klimza et al. | 19 meses | 90 lesiones (44 pacientes) |
100% (79,5% WL) | 0% (20% WL)V |
| 14 | 10.1002/hed.25047 | NBI versus laryngovideostroboscopy | Polonia | 2018 | Rzepakowska et al. | 12 meses | 105 | Premalignas: 98,8% Malignas: 92,9%VI |
Premalignas: 73,9% Malignas: 88,9%VI |
| 15 | 10.1002/hed.25201 | NBI for risk stratification within leukoplakia | Polonia | 2018 | Rzepakowska et al. | No data | 91 lesiones (62 pacientes) |
100% | 97,4% |
| 16 | 10.4103/ijc.IJC_590_17 | Role of NBI in diagnosis of laryngeal lesions | India | 2018 | Sakthivel et al. | 3 meses | 30 | 91,3% NBI 100% NBI+WLVII |
71% NBI 71,4% NBI+WLVII |
| 17 | 10.1111/coa.13361 | Training program for NBI classification | China | 2019 | Ni et al. | 24 meses | 26 | 91% | 75% |
| 18 | 10.1007/s00405-018-5256-1 | Flexible transnasal endoscopy with NBI | Alemania | 2019 | Davaris et al. | 36 meses | 170 lesiones (163 pacientes) |
93% (77% WL) | 97% (97% WL) |
| 19 | 10.5604/01.3001.0013.3401 | Clinical experience with NBI in laryngeal lesions | Polonia | 2019 | Popek et al. | No data | 333 | 98,5% (95,4% WL) | 98,5% (84,2% WL) |
| 20 | 10.1177/0145561320925327 | Diagnostic value of NBI classification | China | 2021 | Lin et al. | 12 meses | 123 lesiones (112 pacientes) |
81%VIII | 84%VIII |
| 21 | 10.1002/lary.29361 | NBI versus conventional white light imaging | Holanda | 2021 | Zwakenberg et al. | 36 meses | 233 lesiones | 92% (86% WL)IX | 85% (87% WL)IX |
Notas:
I: Datos obtenidos en tejidos irradiados y/o tratados con quimioterapia.
II: Diferencia estadísticamente significativa (p < 0,02).
III: Comparación con y sin aplicación de la clasificación de Ni.
IV: Sin datos de sensibilidad/especificidad; incluido por análisis intraoperatorio.
V: No fue posible determinar especificidad por ausencia de falsos positivos.
VI: Análisis diferenciado entre lesiones premalignas y malignas.
VII: Comparación entre WL, NBI y WL+NBI.
VIII: Promedio entre lesiones malignas y premalignas.
IX: Comparación con NBI intraoperatorio rígido.
DISCUSIÓN
El NBI ha demostrado ser útil para la detección de lesiones sincrónicas o metacrónicas, especialmente en pacientes con antecedentes de cáncer de cabeza y cuello. Esta técnica puede identificar tumores que pasarían inadvertidos con la luz blanca convencional. Katada y cols.29 (2008) demostraron que el NBI es eficaz para detectar tumores superficiales en pacientes tratados con quimiorradioterapia, lo que es esencial para el seguimiento posoperatorio y la detección temprana de recurrencias29.
Las clasificaciones de los hallazgos obtenidos con NBI son fundamentales para interpretar las imágenes.
La clasificación de Ni (2011)11 y la de la European Laryngological Society (ELS, 2016)30 son las más utilizadas. La clasificación de Ni divide los patrones vasculares en cinco tipos, desde los benignos (Tipo I y II) hasta los que sugieren malignidad (Tipo V). La especificidad y la sensibilidad para detectar malignidad aumentan considerablemente con las lesiones tipo V, mientras que las lesiones tipo I y II son completamente benignas11. La clasificación de ELS simplifica la interpretación al agrupar las lesiones en dos tipos según la disposición de los vasos: paralelos o perpendiculares al borde libre de la cuerda vocal. Las lesiones con vasos perpendiculares son sospechosas de malignidad y deben ser evaluadas con mayor atención30.
Numerosos estudios han validado la utilidad del NBI para predecir malignidad. En 2015, Bertino y cols. 26 demostraron que el uso sistemático del NBI en la evaluación de lesiones laríngeas aumenta la especificidad y el valor predictivo negativo, lo que reduce la necesidad de biopsias innecesarias26.
Además, el NBI ha demostrado ser particularmente útil para determinar los márgenes quirúrgicos durante la exéresis de tumores. Tanto Garofalo y cols. 32 (2015) como Zwakenberg y cols.31 (2023) encontraron que el uso de NBI intraoperatorio reduce significativamente la tasa de márgenes positivos, lo que disminuye la necesidad de reintervenciones (Fig. 3); en este último trabajo además hallaron mayores recurrencias de enfermedad en pacientes operados solo con la luz blanca tradicional.
Asimismo, en 2021, Lauwerends y cols. 32 establecieron que el uso de NBI intraoperatorio interfiere en las conductas quirúrgicas ya que mejora la visualización de los márgenes tumorales (seguridad oncológica) y la detección de lesiones adicionales. Posicionan a la endoscopia laríngea con NBI como la modalidad más prometedora en la detección intraoperatoria de márgenes y resulta inocua5,22,30. La capacidad del NBI para diferenciar entre lesiones malignas y benignas también es valiosa en procedimientos en consultorio35, donde se pueden realizar biopsias y otros tratamientos sin necesidad de anestesia general. La realización de procedimientos ambulatorios con NBI ha permitido a los pacientes evitar hospitalizaciones y anestesias invasivas, mejorando la calidad de vida y reduciendo los costos. Los procedimientos transnasales guiados por NBI para biopsias en pacientes con antecedentes de cáncer de cabeza y cuello han demostrado ser eficaces y bien tolerados, con resultados histopatológicos precisos y sin complicaciones28.
A pesar de sus múltiples ventajas, el NBI presenta algunas limitaciones. La acumulación de saliva o moco en la mucosa puede dificultar la visualización de los vasos subyacentes, y lesiones como la hiperqueratosis pueden generar un engrosamiento epitelial que dificulta la interpretación. La papilomatosis laríngea es otro desafío importante, ya que las lesiones pueden mostrar patrones vasculares similares a los de tumores malignos, lo que aumenta el riesgo de falsos positivos30.
Es importante destacar que, aunque el NBI es una herramienta poderosa, el procedimiento de referencia (estándar de oro) para el diagnóstico de cáncer de laringe sigue siendo el estudio histopatológico. Ningún método de imagen o endoscopia ha logrado reemplazar el análisis histológico como el principal método diagnóstico. Sin embargo, el NBI representa un avance significativo en la evaluación endoscópica: mejora la precisión diagnóstica, optimiza los márgenes quirúrgicos y reduce la necesidad de procedimientos invasivos.
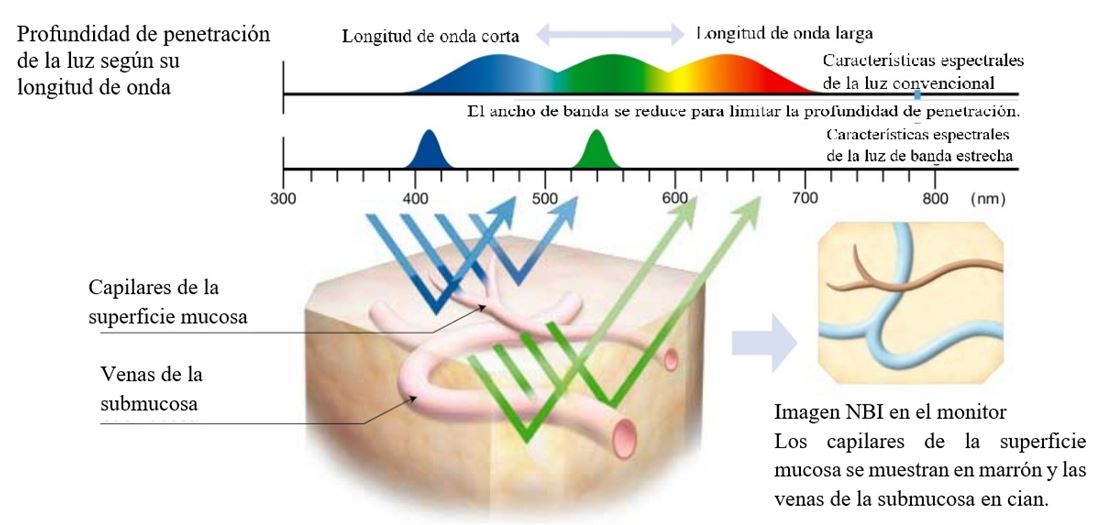
Figura 2. Clasificación de Ni. Desde tipo 1 tipo 5c comparando el tramado vascular con un dibujo, la visualización de las mismas con luz blanca tradicional (WL) y la visualización posterior con el filtro de luz de banda estrecha (NBI) - (Figura tomada de Ni XG, y col.11)
CONCLUSIONES
Como conclusión se destaca una sensibilidad y especificidad alta del NBI para la detección de lesiones premalignas de laringe, siendo superior a la luz blanca convencional.
Asimismo, se demostró que brinda un aporte positivo en su uso intraoperatorio para la determinación de márgenes oncológicos negativos y de esta forma disminuir la posibilidad de recaída tumoral y reintervención quirúrgica.
La clasificación de Ni y la de la ELS están validadas para su uso como análisis de las lesiones laríngeas por NBI con buena aproximación diagnóstica.
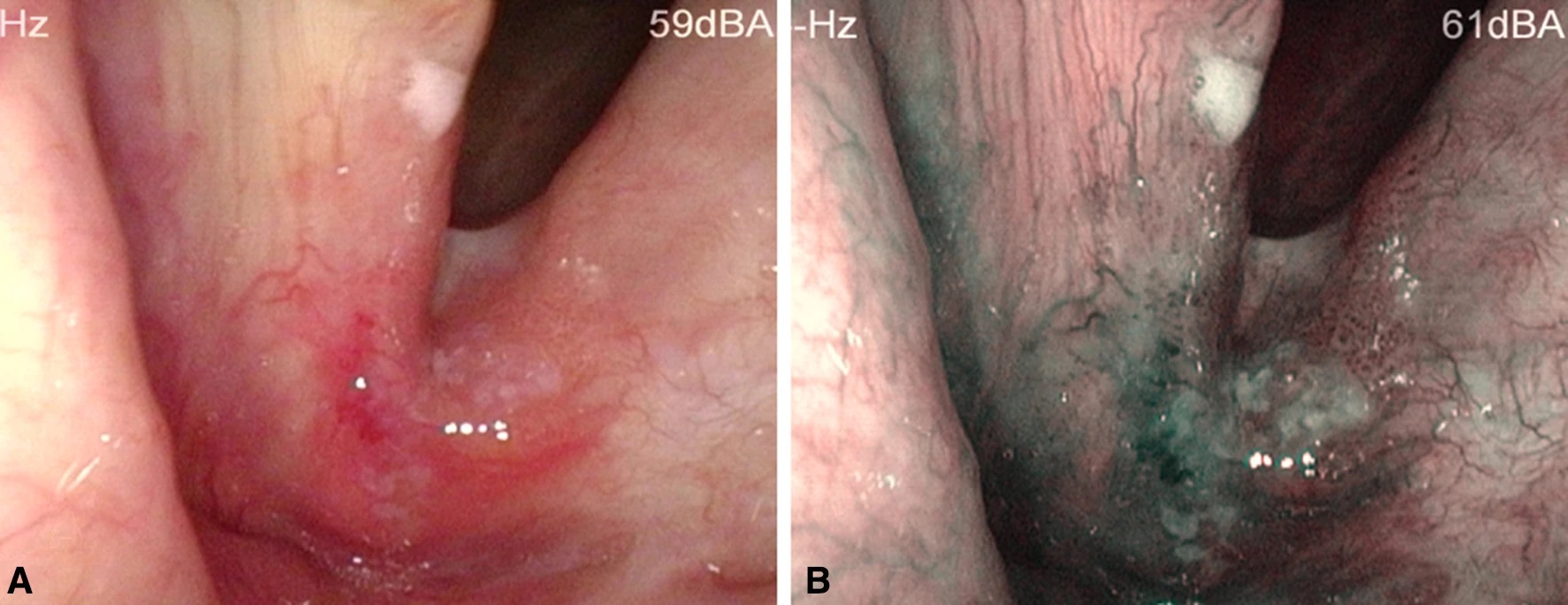
Figura 3. En esta figura se visualiza en la imagen de la izquierda una lesión eritroplásica de comisura anterior bajo WL y en la foto de la derecha se ve la misma lesión bajo NBI pero con mayor extensión que bajo WL (se debe ampliar la resección para obtener márgenes libres) - (Figura tomada de Davaris N. y col.28)
Tabla 2. Datos extraídos de los trabajos analizados
