RESUMEN
Introducción
El exponencial desarrollo de medicamentos innovadores plantea desafíos a los sistemas de salud para garantizar el acceso equitativo a los nuevos tratamientos. En el ámbito hospitalario, los Comités de Evaluación de Medicamentos (CEM) de cada institución analizan la evidencia sobre eficacia, seguridad y costo de los nuevos fármacos para emitir recomendaciones adaptadas a sus contextos específicos. Nuestro objetivo es describir la actividad del CEM en un Hospital Universitario.
Material y métodos
Estudio de corte transversal realizado en un Hospital Universitario. Se analizaron las evaluaciones efectuadas entre los años 2017 y 2023. Se utilizó estadística descriptiva para cuantificar el número de solicitudes de evaluación recibidas, medicamentos incorporados, servicios solicitantes y Clasificación Anatómica, Terapéutica, Química (ATC) de los fármacos.
Resultados
El CEM inició sus actividades en 2011 y está conformado por 13 profesionales de la salud. Durante el período en estudio, se recibieron 111 solicitudes para la incorporación de fármacos, de las cuales 90 (81%) fueron aprobadas e incluidas en el vademécum. El Servicio de Clínica Médica presentó 60 (54%) solicitudes, de las cuales 26 (23%) correspondieron a la Sección de Oncología.
Conclusiones
El CEM tiene un papel central en la incorporación de nuevos fármacos al vademécum institucional, especialmente en áreas críticas como Oncología, atendiendo a la creciente demanda de evaluación de tratamientos innovadores.
Palabras clave: Comité de Farmacia y Terapéutica, Evaluación de Tecnología, Servicio de Farmacia del Hospital, Administración del Hospital, Comités de Medicamentos.
The Experience of a Drug Evaluation Committee at a University Hospital
ABSTRACT
Introduction
The exponential development of innovative drugs poses challenges to healthcare systems in ensuring equitable access to new treatments. At the hospital level, Drug Evaluation Committees (DECs) in each institution analyze the evidence on the effectiveness, safety, and cost of new drugs and make recommendations tailored to their specific contexts. Our objective is to describe the DEC’s activity at a university hospital.
Materials and Methods
This cross-sectional study was undertaken at a university hospital. The evaluations made between 2017 and 2023 were analyzed. We used descriptive statistics to quantify the number of evaluation requests received, the drugs incorporated, requesting departments, and the medications’ ATC classification.
Results
The DEC began its activities in 2011 and is comprised of a team of 13 healthcare professionals. During the study period, 111 requests for drug inclusion were received, of which 90 (81.1%) were approved and incorporated into the institutional formulary. The Internal Medicine Department submitted 60 (54%) requests, 26 (23%) of those came from the Oncology Section.
Conclusions
The DEC plays a central role in incorporating new drugs into the institutional formulary, especially in critical areas such as Oncology, addressing the growing demand for evaluating innovative treatments.
Key words: Pharmacy and Therapeutics Committee, Technology Assessment, Pharmacy Service. Hospital Administration, Drug Committees.
INTRODUCCIÓN
El exponencial desarrollo de medicamentos innovadores y de mayor complejidad tecnológica genera desafíos a los sistemas de salud para garantizar a la población el acceso a nuevos tratamientos. En este contexto son importantes el diseño y la implementación de estrategias que promuevan el uso racional de medicamentos, a fin de asegurar la sostenibilidad del sistema1.
La introducción de estos medicamentos en el mercado comienza con la autorización sanitaria y finaliza con la aplicación terapéutica efectiva a un paciente. En este proceso intervienen distintos organismos que toman decisiones desde niveles macro como los Ministerios de Salud, entidades regulatorias y agencias de evaluación de tecnologías, hasta niveles micro como los comités internos o comités de farmacoterapia hospitalarios2,3.
Existe evidencia de que las herramientas y la información necesarias para la toma de decisiones en los hospitales difieren de aquellas utilizadas en agencias sanitarias de alcance nacional4. Mientras que las agencias nacionales son las responsables de la aprobación de la comercialización, los comités de evaluación de medicamentos (CEM) realizan la evaluación y selección de los medicamentos que conformarán el vademécum de una determinada institución. A su vez, emiten recomendaciones específicas de uso utilizando criterios de racionalidad y eficiencia, contextualizadas en las características particulares de cada institución4. Estos comités están constituidos por equipos multidisciplinarios de profesionales de la salud que deben examinar la evidencia disponible sobre la eficacia, seguridad, calidad y costo de los fármacos para evaluar5,6.
En la Argentina, las decisiones a nivel macro en cuanto a registro de medicamentos y recomendaciones de uso están dadas por el Ministerio de Salud de la Nación, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) y la Comisión Nacional de Evaluación de Tecnologías Sanitarias y Excelencia Clínica (CONETEC). A nivel micro, la toma de decisiones es particular de cada organización, y la modalidad de trabajo adoptada por cada institución no está ampliamente difundida.
Por este motivo, para abordar la falta de documentación y contribuir al conocimiento en el área, nuestro propósito es compartir la experiencia de los últimos 6 años de trabajo del CEM de un hospital universitario de la Ciudad Autónoma de Buenos Aires, Argentina.
OBJETIVOS
Primario
- Describir el funcionamiento del CEM en un hospital universitario.
Secundario
- Cuantificar la actividad del CEM en términos de:
- Número total de solicitudes de evaluación de medicamentos recibidas.
- Número de medicamentos incorporados al vademécum hospitalario luego de la evaluación.
- Servicios y secciones médicas que realizaron las solicitudes de evaluación de medicamentos.
- Tipo de medicamento de acuerdo con la clasificación anatómica, terapéutica y química (ATC)7.
MATERIALES Y MÉTODOS
El estudio se llevó a cabo en el ámbito de un hospital universitario de la Ciudad Autónoma de Buenos Aires, Argentina.
Para el objetivo primario se realizó un análisis descriptivo del procedimiento institucional N.º 045/11: Comité de Evaluación de Medicamentos e Insumos Biomédicos, N.º de Versión/Modificación: 01/01, Fecha de Vigencia: 23/09/2024* .
Para el objetivo secundario, se llevó a cabo un estudio observacional retrospectivo de los informes rápidos elaborados por los integrantes del CEM desde enero de 2017 hasta diciembre de 2023.
Se midieron las siguientes variables:
- Número de solicitudes evaluadas. Se registró la cantidad total de solicitudes de evaluación de medicamentos recibidas durante el período de estudio.
- Número de solicitudes incorporadas y no incorporadas sobre el total de solicitudes recibidas por un año durante el período de estudio.
- Servicio solicitante. Se identificó y clasificó el Servicio del hospital que realizó cada solicitud.
- Tipo de fármaco. Se categorizó cada medicamento solicitado de acuerdo con la clasificación ATC7.
Para el análisis de los datos se empleó estadística descriptiva. Las variables cuantitativas (número de solicitudes, número de solicitudes incorporadas y no incorporadas) y las variables cualitativas (Servicio solicitante, tipo de fármaco) se resumieron mediante frecuencia absoluta y relativa (porcentaje).
* Comunità - Hospital Italiano [Internet]. [cited 2024 Aug 13]. Available from: https://intranet.hospitalitaliano.org.ar/normasprocedimientos
CONSIDERACIONES ÉTICAS
Dado que este trabajo es una revisión de evaluaciones sin la inclusión de datos de pacientes ni información que permita su identificación, no fue necesario obtener la aprobación del Comité de Ética para Protocolos de Investigación.
RESULTADOS
El CEM del Hospital depende de la Dirección Médica, quien nombra a sus integrantes. Inició sus actividades en el año 2011, momento en el cual estaba constituido por un médico, una farmacéutica y una administrativa. Actualmente está integrado por 13 profesionales de la salud, entre los que se encuentran farmacéuticos y médicos. La descripción de su funcionamiento puede observarse en la figura 1.
Durante el período de estudio 2017-2023 se recibieron 111 solicitudes de incorporación de fármacos de las cuales 90 (81%) fueron incorporadas al vademécum.
En el período 2022-2023 se recibieron 50 solicitudes que representan el 45% de la totalidad de solicitudes recibidas durante el período del estudio. En la figura 2 se presenta el número de solicitudes totales y las incorporadas y no incorporadas al vademécum hospitalario para cada año.
Los Servicios que solicitaron evaluación de fármacos en el período 2017-2023 se observan en la tabla 1.
Las solicitudes de nuevas incorporaciones, según la clasificación ATC pueden observarse en la figura 38.
Los fármacos evaluados e incorporados al vademécum hospitalario se observan en el Anexo 3.
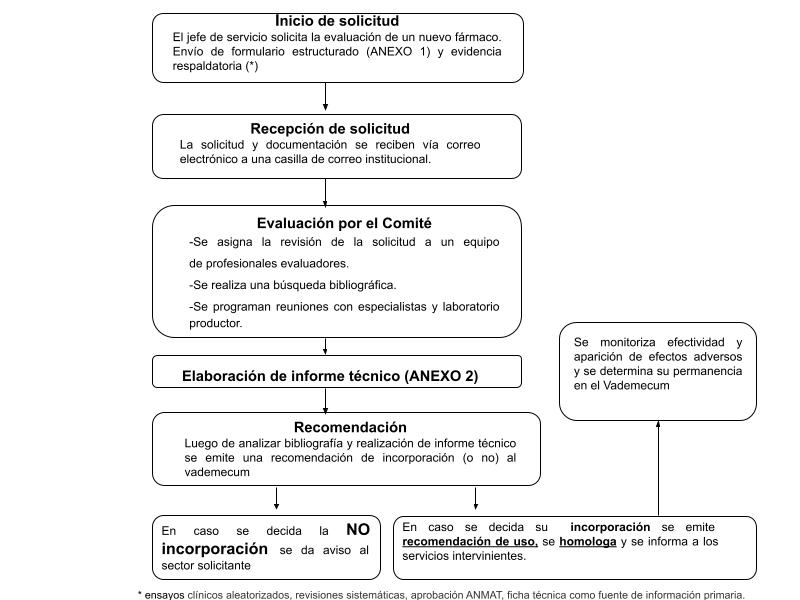
Figura 1.Descripción del funcionamiento del Comité de Evaluación de Medicamentos.
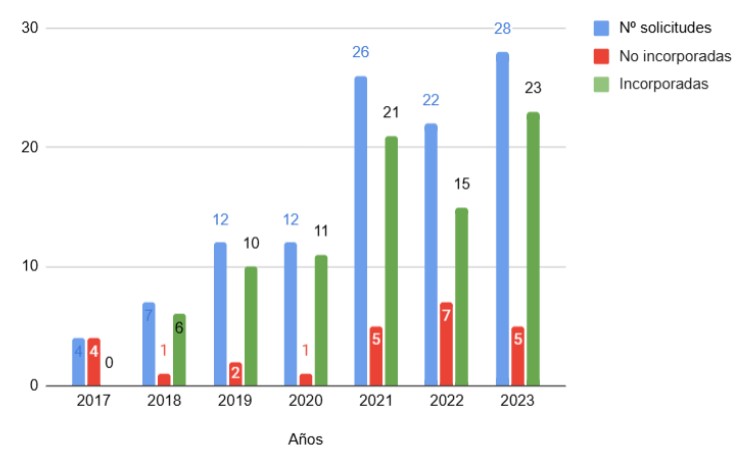
Figura 2.Número de solicitudes totales, no incorporadas e incorporadas por año.

Tabla 1.Servicios médicos que solicitaron evaluación de fármacos.
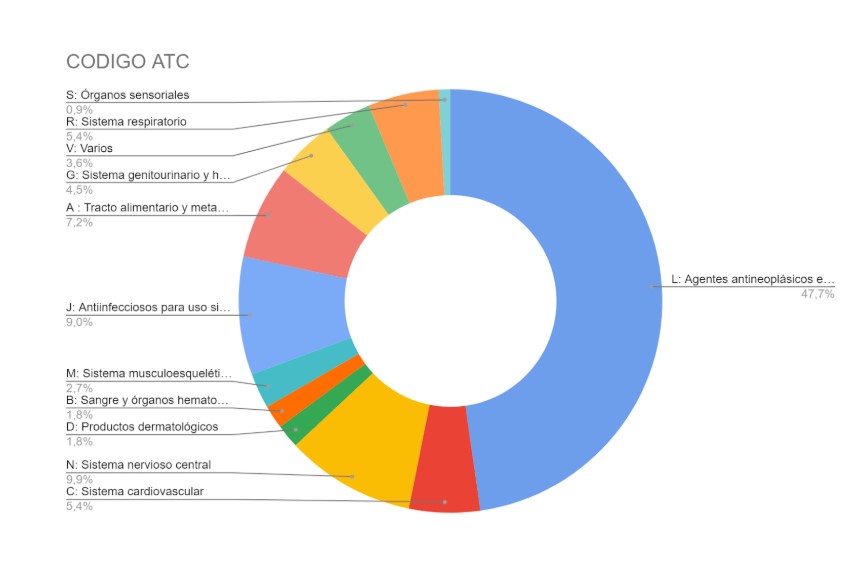
Figura 3.Solicitudes de fármacos según clasificación ATC.
DISCUSIÓN
En nuestro estudio describimos la composición del CEM en la red integrada de un hospital universitario que, estructuralmente, cumple con algunos de los componentes descriptos por el subgrupo de estudio del Hospital Based Health Technology Assessment (HB-HTA)4.
Siguiendo los modelos propuestos por este subgrupo de HB-HTA, nuestro comité se encuadra en la descripción de un comité interno compuesto por un grupo multidisciplinario de profesionales de salud de la organización que no desempeñan funciones exclusivas dentro del comité5.
En la Argentina funcionan en diferentes organizaciones equipos de trabajo o comités que realizan evaluación de tecnologías en cada institución. Sin embargo, no identificamos bibliografía publicada que describa el funcionamiento y resultados de esas evaluaciones.
Como fortaleza del trabajo del CEM, cada fármaco es evaluado y analizado críticamente con apoyo de la evidencia científica disponible, con la correspondiente evaluación de su impacto presupuestario. Esto permite una gestión adecuada de la utilización de los medicamentos, según criterios de seguridad y eficacia bajo una monitorización continua.
Entre los desafíos de este tipo de comité, la dedicación parcial de los miembros condiciona el tiempo dedicado para esta actividad. Otra característica de nuestro CEM es que las recomendaciones solo abarcan la red del Hospital (sus diferentes sedes y centros periféricos) y no se extienden ni se comparten con otras organizaciones de salud. Esto representa un limitante en la eficiencia de los recursos, al favorecer la duplicación innecesaria de esfuerzos en la evaluación y análisis de la evidencia4.
En relación con cuantificar la actividad del CEM, es relevante establecer un marco de referencia en el ámbito nacional. En la Argentina, la CONETEC es el organismo que realiza evaluaciones y emite recomendaciones técnicas sobre la incorporación, desinversión, forma de uso, financiamiento y cobertura de las tecnologías9. Estas recomendaciones de la CONETEC son incorporadas como parte del cuerpo de evidencia que sustenta el informe final del CEM y se adaptan a las necesidades específicas del Hospital10.
En nuestro estudio observamos que la mayor proporción de fármacos evaluados corresponden a la clasificación ATC de antineoplásicos e inmunomoduladores (clasificación L) y representan un 47,7% del total de evaluaciones. Analizando el mismo período, en los informes de CONETEC esta categoría representa el 42%. Estos resultados son similares y reflejan una tendencia compartida en la evaluación de este tipo de medicamentos.
Según nuestros resultados, en el bienio 2022-2023 se observa un incremento en el número de solicitudes que recibió el CEM, lo que representa el 45% del total solicitado en el período de estudio (2017-2023). La Sección de Oncología es la que registró el mayor número de solicitudes, en concordancia con la mayor disponibilidad de nuevas terapias oncológicas en el mercado. Un artículo de revisión sobre nuevas indicaciones en oncología aprobadas por la agencia sanitaria Food and Drug Administration de Estados Unidos (FDA) informa una tasa de aprobación de 56 nuevos fármacos anuales entre 2017 y 2022, en comparación con años anteriores, cuando la tasa de aprobación era considerablemente menor11. Este aumento en las evaluaciones de terapias oncológicas podría deberse al rápido desarrollo de nuevos tratamientos y a la creciente demanda de los equipos clínicos por acceder a ellos. La oncología es un área con alta presión asistencial y fuerte impacto clínico, lo que genera un aumento en las solicitudes al CEM para analizar la evidencia y justificar su incorporación.
En esta discusión nos centramos en los puntos para los cuales se dispone de datos de referencia, los cuales son limitados en el ámbito regional. Esta limitación resalta la necesidad de continuar generando y compartiendo información a fin de favorecer el desarrollo de estrategias para la toma de decisión basadas en evidencia en el ámbito hospitalario.
CONCLUSIONES
El uso racional de medicamentos es un desafío transversal en todos los niveles de atención en salud, y la presencia de un Comité de Evaluación de Medicamentos (CEM) hospitalario resulta clave para promover una utilización más eficiente de los recursos disponibles, adaptándose al contexto y las particularidades de cada institución. Nuestro estudio presenta la experiencia acumulada durante seis años de funcionamiento del CEM, documentando su estructura, metodología de trabajo y número de evaluaciones. Al visibilizar y cuantificar su actividad, este trabajo contribuye al conocimiento regional, ofreciendo un modelo de referencia para la gestión sanitaria en otros contextos.

Anexo 1.Formulario de solicitud de evaluación de nuevos fármacos.

Anexo 2.Estructura de Informe Técnico utilizado por el CEM.
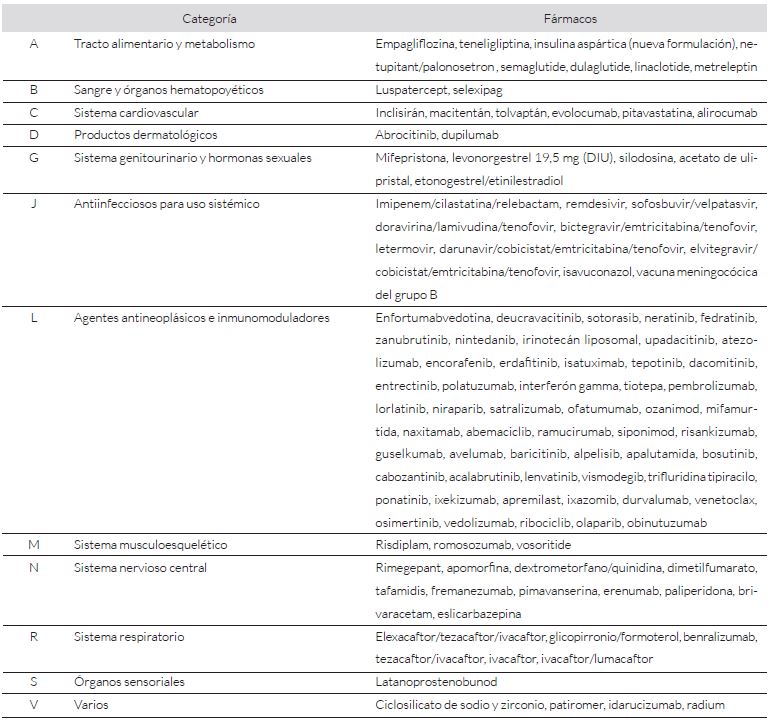
Anexo 3.Fármacos evaluados e incorporados al vademécum hospitalario.