RESUMEN
Introducción
El COVID persistente es una condición médica que afecta a individuos que han padecido COVID-19, cuyos síntomas perduran más allá de tres meses posteriores al cuadro agudo. La Organización Mundial de la Salud (OMS) lo define como un síndrome multisistémico que compromete aparatos como el respiratorio, cardiovascular, neurológico y gastrointestinal, y afecta considerablemente la calidad de vida. Entre los síntomas más comunes se incluyen fatiga extrema, dificultad para respirar, trastornos cognitivos, alteraciones del sueño y dolor muscular.
Estado del arte
Aunque los mecanismos exactos no están completamente esclarecidos, se han identificado varias posibles causas, como la persistencia viral, la inflamación crónica y la disfunción mitocondrial. El desequilibrio inmunológico constituye un factor central, ya que una respuesta exacerbada del sistema inmunitario genera un estado inflamatorio persistente. La sobreproducción de citocinas, como la interleucina-6 (IL-6), junto con procesos autoinmunes, contribuye al daño tisular prolongado. Asimismo, los pacientes con comorbilidades, antecedentes de enfermedad grave, o falta de vacunación presentan mayor riesgo de desarrollar COVID persistente.
La microbiota también desempeña un papel relevante. Su alteración (disbiosis) podría amplificar la inflamación sistémica y los síntomas neurológicos. Varias investigaciones recientes exploran la modulación de la microbiota a través de probióticos, como posible estrategia terapéutica. No obstante, los estudios clínicos se encuentran en fases iniciales. De manera paralela, algunos antivirales e inmunomoduladores están siendo evaluados, aunque aún no existe un tratamiento estandarizado. Pese a estas limitaciones, la vacunación se ha mostrado eficaz en reducir tanto la incidencia de COVID persistente, como la gravedad de sus manifestaciones. Actualmente, múltiples estudios internacionales buscan identificar factores de riesgo, biomarcadores diagnósticos y nuevas opciones terapéuticas.
Discusión
El COVID persistente representa un desafío sanitario de gran magnitud que exige respuestas coordinadas.
Conclusión
La revisión de los mecanismos patogénicos, la implicación inmunológica y las posibles estrategias terapéuticas ponen de relieve la necesidad de un abordaje multidisciplinario que integre investigación básica, clínica y epidemiológica. Solo mediante este enfoque será posible avanzar hacia diagnósticos más precisos y tratamientos eficaces que mejoren la calidad de vida de los pacientes afectados.
Palabras clave: COVID persistente, SARS-CoV-2, inflamación, disbiosis, vacunación, antivirales, biomarcadores, secuelas neurológicas.
Long-COVID: Advances in Diagnostics, Biomarkers and Innovative Therapies
ABSTRACT
Introduction
Long COVID is a medical condition that affects individuals who have had COVID-19 and whose symptoms persist beyond three months after the acute phase. The World Health Organization (WHO) defines it as a multisystem syndrome that affects systems such as the respiratory, cardiovascular, neurological, and gastrointestinal systems, and significantly affects quality of life. The most common symptoms include extreme fatigue, shortness of breath, cognitive disorders, sleep disturbances, and muscle pain.
State of the art
Although the exact mechanisms are not fully understood, several possible causes have been identified, such as viral persistence, chronic inflammation, and mitochondrial dysfunction. Immune imbalance is a central factor, as an exacerbated immune system response generates a persistent inflammatory state. Overproduction of cytokines, such as interleukin-6 (IL-6), along with autoimmune processes, contribute to prolonged tissue damage. Furthermore, patients with comorbidities, a history of severe illness, or lack of vaccination are at higher risk of developing Long COVID. The microbiota also plays a relevant role. Its alteration (dysbiosis) could amplify systemic inflammation and neurological symptoms. Recent research explores microbiota modulation through probiotics as a possible therapeutic strategy. However, clinical studies are in their initial stages. In parallel, some antivirals and immunomodulators are being evaluated, although there is still no standardized treatment. Despite these limitations, vaccination has proven effective in reducing the incidence of Long-COVID, as well as the severity of its manifestations. Currently, multiple international studies seek to identify risk factors, diagnostic biomarkers, and new therapeutic options.
Discussion
Long-COVID represents a major health challenge that requires coordinated responses.
Conclusion
A review of the pathogenetic mechanisms, immunological implications, and potential therapeutic strategies highlights the need for a multidisciplinary approach that integrates basic, clinical, and epidemiological research. Only through this approach will it be possible to move toward more accurate diagnoses and effective treatments that improve the quality of life of affected patients.
Key words: Long-COVID, SARS-CoV-2, inflammation, dysbiosis, vaccination, antivirals, biomarkers, neurological sequelae.
INTRODUCCIÓN
La Organización Mundial de la Salud (OMS) define el COVID persistente como una “condición post-COVID-19” cuando los síntomas subsisten más de tres meses tras la infección, sin diagnóstico alternativo. Afecta a diversos sistemas, especialmente al pulmonar1,2.
Los síntomas comunes son dificultad para respirar, fatiga, obnubilación mental, anosmia, pérdida de cabello, disfunción sexual y alteración del sueño3.
Factores como enfermedad grave por COVID-19, condiciones preexistentes, ausencia de vacunación, infecciones repetidas, género, tabaquismo y edad aumentan el riesgo1-3.
La infección con diferentes variantes del SARS-CoV-2 se asocia a distintos fenotipos patológicos. La variante ómicron presenta menor riesgo en comparación con la original y la delta3.
El objetivo de esta revisión es analizar las características clínicas, inmunológicas y transcriptómicas del COVID persistente, así como los mecanismos patogénicos propuestos, los factores de riesgo, los posibles biomarcadores y los avances terapéuticos. De este modo, se busca aportar una base científica actualizada que contribuya a la comprensión integral de esta condición y favorezca la implementación de un enfoque multidisciplinario en su diagnóstico, prevención y tratamiento.
ESTADO DEL ARTE
Mecanismos patogénicos y compromiso inmunológico
Los mecanismos patogénicos del COVID persistente incluyen la subsistencia del virus o sus componentes en los tejidos, lo que provoca inflamación crónica, respuestas autoinmunes desreguladas, disfunción mitocondrial y endotelial, y disbiosis de la microbiota. También se ha observado la reactivación de virus inactivos, como el Epstein-Barr y varicela zóster, así como disfunción cerebral, neuroendocrina y alteraciones en la coagulación3,4.
Sin embargo, el desarrollo de esta condición aún no está completamente definido.
En relación con los mecanismos inmunológicos que podrían estar involucrados se describen distintos mediadores inmunes y biomarcadores circulantes, como el cortisol, la serotonina, las interleucinas 8, 4 y 6 , la quimiocina proteína inflamatoria de macrófagos beta y la linfopoyetina estromal tímica (IL-8,IL-4, IL-6, CCL4 y TSLP por sus siglas en inglés)5 .
Múltiples estudios han evidenciado que la IL-6 contribuye a una respuesta antiviral inadecuada, persistencia viral e inflamación a largo plazo característica del COVID persistente. Esta se encuentra relacionada con la lectina de unión a manosa (MBL por sus siglas en inglés), que presenta un papel importante en la neutralización del SARS-CoV-2. Por lo tanto, bajos niveles de MBL podrían contribuir potencialmente a la sobreproducción desregulada de IL-6 y a la gravedad de la enfermedad5.
Los pacientes con deterioro inmunológico preexistente presentan dificultades para eliminar los reservorios de virus residuales o las células infectadas. De esta forma, la persistencia viral puede contribuir a la inflamación continua y a la disfunción cognitiva debido al comportamiento de la enfermedad5 .
El sistema inmunológico de los pacientes con COVID persistente está excesivamente alerta, lo que puede generar respuestas inmunitarias inapropiadas, inflamación crónica, daño tisular y enfermedades autoinmunes6. Se ha propuesto que mecanismos autoinmunes, como la formación excesiva de trampas extracelulares de neutrófilos, están involucrados. Las enfermedades autoinmunes asociadas incluyen el síndrome de Guillain-Barré, la encefalitis autoinmune, la tiroiditis de Hashimoto y la vasculitis7 .
Síntomas
Los síntomas persistentes del COVID persistente afectan la calidad de vida e incluyen fatiga extrema, deterioro cognitivo, taquicardia, pérdida del olfato/gusto, insomnio, ansiedad, depresión, dificultad respiratoria, hipoacusia, edema y problemas gastrointestinales. Es crucial que los pacientes reciban atención médica multidisciplinaria para desarrollar un tratamiento personalizado8.
Los casos son más comunes en adultos; sin embargo, algunos estudios recientes realizados en niños y adolescentes identificaron que el 25% presentó más de 40 síntomas atribuibles a esta patología9,10. Entre los síntomas más frecuentes se encuentran alteraciones del estado de ánimo, como tristeza, ansiedad, tensión, ira o depresión (16,50%), seguidas de fatiga (9,66%), problemas de sueño (8,42%), dolores de cabeza (7,84%), síntomas respiratorios (7,62%), congestión nasal (7,53%) y dificultades cognitivas, como problemas de concentración, confusión, dificultades de aprendizaje y pérdida de memoria (6,27%)10,11.
Vacunación contra COVID-19
Las vacunas contra el COVID-19 han demostrado ser eficaces no solo en la prevención de infecciones graves, sino también en la reducción del riesgo de COVID persistente. Diversos estudios en países como el Reino Unido, España y Estonia muestran que las personas vacunadas tienen menor incidencia de síntomas prolongados12,13.
En la Argentina, ciertas vacunas como BBIBP-CorV® (Sinopharm), BNT162b2® (Pfizer) y mRNA-1273® (Moderna) fueron eficaces en la prevención de hospitalizaciones y de síntomas persistentes durante el brote de ómicron14.
Algunas investigaciones en Corea del Sur y Estados Unidos también indican que los vacunados experimentan síntomas menos graves y de menor duración4,15.
A pesar de estos avances, los mecanismos subyacentes siguen siendo complejos y multifactoriales, por lo que continúan los esfuerzos para desarrollar terapias específicas1 . La vacunación sigue siendo la intervención más eficaz y accesible para reducir el impacto, consolidándose como una estrategia clave no solo para prevenir infecciones agudas, sino también para mitigar las consecuencias a largo plazo.
Tratamiento
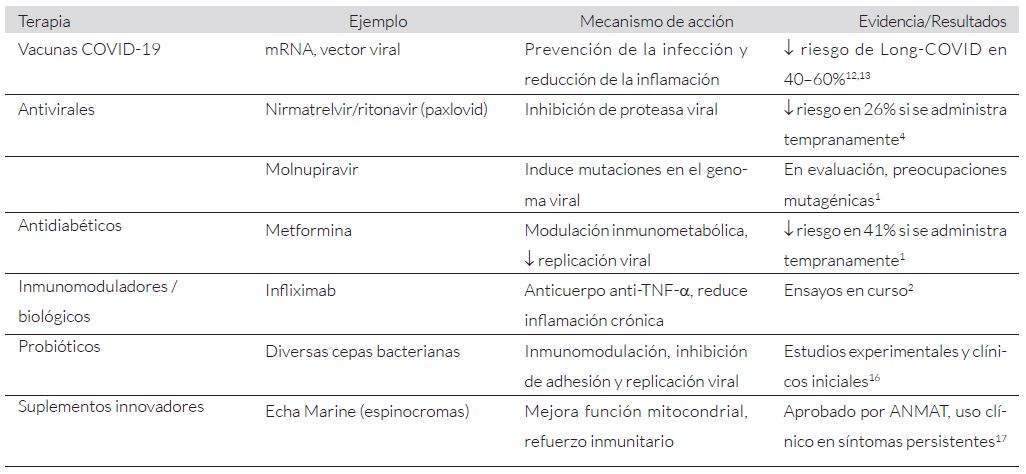
La vacunación reduce el riesgo de COVID persistente en un 40-60%, pero no lo elimina por completo, lo que ha impulsado la investigación de terapias más específicas12,13. Actualmente, no existe un tratamiento aprobado, pero se están evaluando varios medicamentos en ensayos clínicos (Tabla 1).
El antiviral nirmatrelvir/ritonavir (paxlovid) ha demostrado reducir el riesgo en un 26% si se administra en los primeros cinco días de la infección4. Otro antiviral en estudio es el molnupiravir, aunque su uso genera preocupaciones debido a sus efectos mutagénicos1 . La metformina, usada principalmente para la diabetes tipo 2, también muestra potencial al reducir el riesgo en un 41% si se administra tempranamente1 .
La disfunción inmunológica observada en pacientes ha llevado también a explorar el uso de fármacos inmunomoduladores para reducir la inflamación crónica y los efectos a largo plazo de la infección por SARS-CoV-2. Por ejemplo, uno de los biofármacos que los National Institutes of Health (NIH) probaron fue infliximab2.
Además, se investigan probióticos como adyuvantes inmunomoduladores con efectos antivirales. Incluso se descubrió que algunas especies y cepas probióticas ejercen mecanismos de acción antivirales como por ejemplo inhibición competitiva de la adherencia viral o su replicación16.
Echa Marine®, un suplemento dietario clínicamente testeado y aprobado por ANMAT (Administración Nacional de Medicamentos, Alimentos y Tecnología Médica-Registro Nacional de Producto Alimenticio RNPA 07-007419), está diseñado para aliviar los síntomas del COVID persistente. Desarrollado por ERISEA S.A. con tecnología argentina, utiliza espinocromas de erizos de mar para mejorar la función mitocondrial y fortalecer el sistema inmunitario, destacando el potencial de la ciencia nacional para abordar problemas de salud global17.
Microbiota intestinal
Diversos estudios han mostrado una relación entre la microbiota intestinal y el COVID persistente. En estos pacientes se ha observado disbiosis, con una disminución de bacterias beneficiosas como Faecali bacterium prausnitzii, y un aumento de patógenos como Enterobacteriaceae.
El receptor ACE2 en las células intestinales facilita la entrada del SARS-CoV-2, lo que provoca alteraciones en la microbiota y síntomas gastrointestinales, como diarrea, náuseas y dolor abdominal, al afectar la integridad de la barrera intestinal y permitir la translocación bacteriana al torrente sanguíneo, desencadenando inflamación18,19.
La disbiosis también puede influir en la inflamación central a través del eje intestino-cerebro, afectando el deterioro cognitivo y otros síntomas neurológicos, especialmente en ancianos20.
El uso de probióticos y sus metabolitos puede restaurar la microbiota intestinal, regular la barrera intestinal y modular el sistema inmunológico, reduciendo el estrés inflamatorio y oxidativo 19,21. La suplementación con simbióticos (combinación de prebióticos y probióticos) puede aliviar síntomas como diarrea, disnea y deterioro cognitivo, mostrando un enfoque prometedor para mitigar los efectos de la patología. Sin embargo, se necesitan más estudios para comprender el mecanismo exacto por el cual la microbiota influye en la recuperación22.
La modulación de la microbiota intestinal puede ejercer efectos antivirales indirectos en la infección por SARS-CoV-2, ayudando en la reparación de la barrera intestinal y en los procesos antiinflamatorios. Algunos probióticos también muestran efectos antivirales directos, bloqueando la adhesión y replicación viral23.
Tabla 1. Resumen de tratamientos en estudio para COVID persistente.
Estudios transcriptómicos
La transcriptómica estudia el conjunto completo de ácido ribonucleico (ARN), desde micro-ARN hasta ARN largos no codificantes, permitiendo entender cómo un solo genoma genera diferentes tipos de células y regula la expresión génica. Las técnicas principales incluyen microarreglos (microarrays), que cuantifican secuencias predeterminadas, y la secuenciación de ARN (RNA-Seq) mediante técnicas como la Secuenciación de Nueva Generación (NGS), que permite un análisis exhaustivo de todos los transcriptos.
El estudio del transcriptoma es clave no solamente para la interpretación de elementos funcionales del genoma, sino también para comprender el origen y desarrollo de diversas enfermedades24.
La publicación del genoma humano a principios de los 2000 ha influido enormemente en esta ciencia.
Además, el avance de la bioinformática y las herramientas de mapeo de secuencias han hecho posible no solo la detección de partes de los transcriptos, sino también la reconstrucción de sus secuencias24.
En pacientes con COVID persistente se ha detectado ARN persistente del SARS-CoV-2, lo que sugiere que la replicación viral residual contribuye a los síntomas persistentes. Un estudio de Soraya Maria Menezes y cols. identificó biomarcadores asociados a síntomas como ansiedad y depresión25. El análisis transcriptómico, mostró la presencia de ARN del virus, especialmente en genes como el de la proteína nucleocápside (N), ORF7a, ORF3a, y un ARN antisentido de ORF1ab, lo que indica replicación viral activa. Asimismo, estos pacientes mostraron una disminución en la actividad inmunometabólica25.
Diversos estudios han demostrado que personas con una infección prolongada por COVID-19 tienen un 50% más de probabilidades de desarrollar esta patología que las personas con infección no persistente. En algunos individuos se han identificado sustituciones de aminoácidos virales que incluyeron mutaciones en diferentes variantes del SARS-CoV-2. Por ejemplo, mutaciones recurrentes en individuos inmunodeprimidos y mutaciones con propiedades para evadir la respuesta inmunitaria26.
Biomarcadores
Estados Unidos ha invertido 1500 millones de dólares en estudios sobre COVID persistente, buscando biomarcadores pronósticos y terapéuticos. Cuarenta y cuatro (44) de sus 50 estados han abierto clínicas especializadas para pacientes con COVID largo, y otros países han seguido su ejemplo. Esta investigación es fundamental para mejorar el manejo clínico y comprender las secuelas a largo plazo de las infecciones virales27.
Biomarcadores salivales en niños
La saliva se ha propuesto como una matriz biológica prometedora para estudiar los cambios fisiológicos asociados al COVID persistente en niños, debido a su fácil recolección, procedimiento seguro y no invasivo28. Un estudio reciente de Tyrkalska y cols. analizó muestras de saliva de 49 niños enfermos y 56 controles sanos del mismo rango etario, evaluando 13 biomarcadores seleccionados por su capacidad para reflejar el estado redox, la respuesta inmunitaria, el estrés agudo y el estado homeostático general29 (Tabla 2).
En los niños con sintomatología se observó un aumento en los biomarcadores oxidantes TOS y d-ROM, mientras que los antioxidantes TEACH, CUPRAC y FRAP se redujeron significativamente, indicando un desequilibrio redox. Sin embargo, AOPP no mostró variaciones notables. En cuanto a la respuesta inmunitaria, solo ADA2 y tADA presentaron cambios significativos. Además, los niveles de sAA y proteínas totales se encontraron disminuidos.
Los resultados indican que los niveles de la mayoría de los biomarcadores salivales y los patrones de correlación difieren significativamente entre los niños con COVID persistente y los controles. Esta información podría ser útil para distinguir entre ambos grupos. En particular, la combinación de TOS, ADA2, proteínas totales y AOPP permitiría una distinción fiable, mientras que las proteínas totales y ADA1 podrían diferenciar entre síntomas leves y graves. Además, se encontró que los niveles de biomarcadores salivales están correlacionados con parámetros demográficos y clínicos en esta población.
Biomarcadores de compromiso neurológico
Otro grupo de biomarcadores en estudio son las vesículas extracelulares derivadas de neuronas (nEVs, por sus siglas en inglés). Estas nanopartículas secretadas por células neuronales contienen proteínas específicas que reflejan el estado fisiológico o patológico de las células que las producen30. Las nEVs se aíslan del plasma mediante un proceso de purificación con anticuerpos monoclonales anti-L1CAM, lo que permite realizar estudios específicos sobre enfermedades neurológicas.
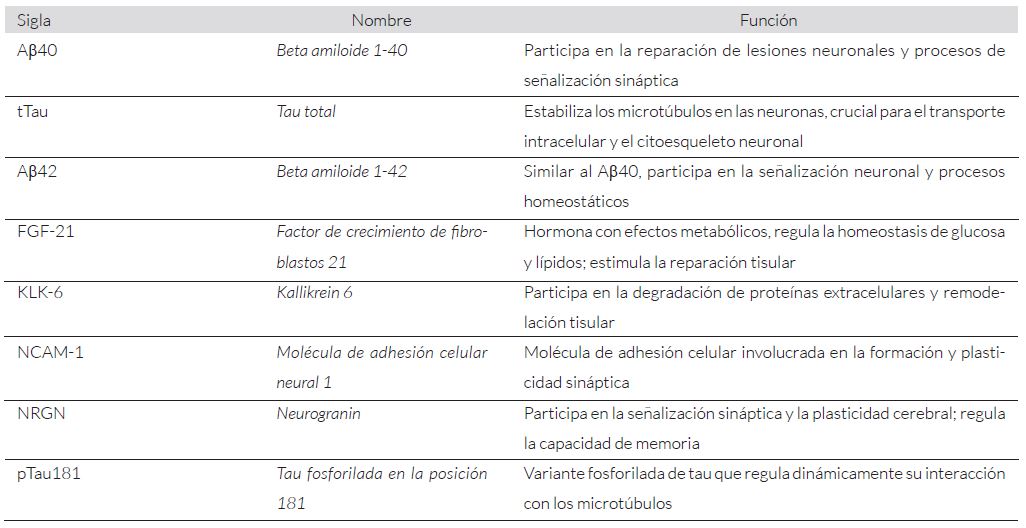
La relevancia de estas vesículas radica en su capacidad para actuar como biomarcadores en enfermedades cerebrales, especialmente en condiciones donde cruzan la barrera hematoencefálica y llevan señales de alteraciones neuronales, como en el caso de las secuelas neuronales del COVID persistente, manifestando proteínas indicativas de disfunción neuronal, como beta-amiloide y pTau181, entre otras (Tabla 3)30.
Las consecuencias neuronales del COVID persistente incluyen una serie de síntomas que afectan el sistema nervioso de los pacientes recuperados de la fase aguda del COVID-19. Estos síntomas incluyen fatiga crónica, niebla cerebral, trastornos del sueño, dolores de cabeza persistentes, trastornos del estado de ánimo y alteraciones sensoriales30.
En un estudio realizado por Tang N y cols., se analizaron los niveles de proteínas en las nEVs de tres grupos: pacientes con secuelas neurológicas, pacientes recuperados sin síntomas persistentes y controles sanos previos a la pandemia. Se observó que todas las proteínas analizadas, excepto Aβ40, estaban significativamente elevadas en las nEVs de los pacientes con secuelas neurológicas en comparación con los controles sanos previos a la pandemia. Sin embargo, en los pacientes recuperados sin síntomas, Aβ40 estuvo significativamente elevada en comparación con los controles.
Además, las nEVs de pacientes con secuelas neurológicas presentaron niveles significativamente elevados de proteínas neuronales, incluyendo Aβ42, FGF-21, KLK-6, NCAM-1, NRGN, pTau181, TDP-43, tTau y HMGB1, en comparación con los controles sanos previos a la pandemia30.
En conclusión, los pacientes de COVID persistente con secuelas neurológicas mostraron una elevación significativa de proteínas relacionadas con neurodegeneración. En el grupo de pacientes recuperados sin síntomas, las diferencias fueron menos marcadas, lo que indica la relevancia específica de estos biomarcadores30.
Tabla 2. Biomarcadores salivales seleccionados para el estudio de Long-COVID en niños.
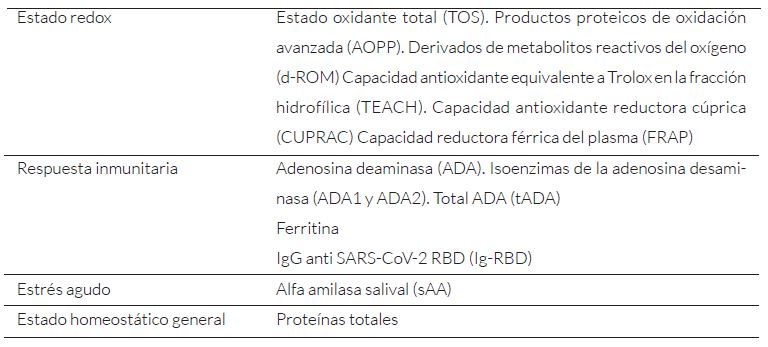
Tabla 3. Función de las proteínas medidas en las vesículas extracelulares derivadas de neuronas (nEVs,por sus siglas en inglés).
DISCUSIÓN
El COVID persistente, caracterizado por la permanencia de síntomas más allá de tres meses tras la infección aguda por SARS-CoV-2, plantea desafíos significativos debido a su amplia heterogeneidad clínica y las múltiples vías patogénicas implicadas. Los mecanismos subyacentes, como la persistencia viral, la disfunción inmunológica, la inflamación crónica y las alteraciones en la microbiota intestinal, han sido ampliamente estudiados.
Estos procesos están relacionados con la reactivación de virus latentes, la inflamación vascular y neuronal, así como con alteraciones neuroendocrinas y del sistema inmunológico. Asimismo, la desregulación de citocinas clave como la IL-6, desempeña un papel importante en la progresión de la patología, especialmente en pacientes con condiciones preexistentes o deterioro inmunológico.
Los síntomas, como fatiga, disfunción cognitiva y trastornos respiratorios, afectan significativamente la calidad de vida de los pacientes, lo que exige un abordaje médico integral y multidisciplinario. Varias investigaciones recientes han señalado que esta condición también afecta a niños y adolescentes, con síntomas predominantemente relacionados con el estado de ánimo y dificultades cognitivas. Este panorama refuerza la importancia de las estrategias de prevención como la vacunación, que no solo reduce la gravedad de la infección aguda, sino también disminuye el riesgo de desarrollar COVID persistente. Sin embargo, las vacunas por sí solas no eliminan completamente el riesgo, lo que resalta la necesidad de explorar terapias específicas. Los avances terapéuticos incluyen antivirales como el nirmatrelvir/ritonavir y han mostrado resultados prometedores en la reducción de los síntomas cuando se administran en etapas tempranas de la infección. Además, fármacos como la metformina, inmunomoduladores y probióticos han emergido como herramientas potenciales en el manejo de esta condición, aunque se requieren más estudios para confirmar su eficacia y seguridad a largo plazo.
La microbiota intestinal desempeña un papel crucial en la fisiopatología del COVID persistente, ya que la disbiosis intestinal no solo afecta la integridad de la barrera intestinal, sino también contribuye a la inflamación sistémica y a síntomas neurocognitivos. Así, la modulación del microbioma mediante simbióticos se perfila como un tratamiento prometedor, aunque aún se encuentra en una fase inicial de investigación.
CONCLUSIÓN
El COVID persistente es una condición multifactorial con implicaciones significativas para la salud global. A pesar de los avances en la comprensión de sus mecanismos y las opciones terapéuticas emergentes, aún existen importantes brechas en el conocimiento. El desarrollo de estrategias preventivas y terapias específicas, junto con enfoques multidisciplinarios que incluyan el manejo integral de los síntomas, es esencial para abordar esta condición. Además, el apoyo a la investigación científica, como lo demuestra el potencial de innovaciones nacionales como el suplemento dietario Echa Marine, subraya la necesidad de continuar fomentando el avance del conocimiento para mejorar la calidad de vida de los pacientes.